Розвиток мультифокального асептичного остеонекрозу в пацієнта із дерматоміозитом як ускладнення глюкокортикоїдної терапії
Головач І.Ю., Чіпко Т.М., Михальченко О.М.
Резюме. Представлено опис клінічного випадку розвитку асептичного некрозу колінного суглоба та кісток зап’ястка у пацієнта із дерматоміозитом із застосуванням глюкокортикоїдів. Клінічні прояви асептичного некрозу кісток у вигляді інтенсивного больового синдрому розвинулися більше ніж через 1 рік від початку глюкокортикоїдної терапії. За цей період пацієнт отримував перорально преднізолон у стартовій дозі 60 мг/добу за низхідною схемою та курси пульс-терапії метилпреднізолоном (по 500 мг довенно крапельно 3 дні підряд на місяць). Різкий, нестерпний, переважно нічний біль у правому колінному суглобі з’явився після другого курсу пульс-терапії на фоні низької активності дерматоміозиту та значного покращення загального стану пацієнта. Після проведення магнітно-резонансної томографії (МРТ) правого колінного суглоба верифіковано зміни, що відповідали інфарктам правої стегнової та великогомілкової кісток. Через 4 міс після першого епізоду остеонекрозу на фоні остеотропної та судинної терапії виявлено асептичний некроз кісток зап’ястка правої кисті. Поява болю у суглобах, насамперед у колінних і кульшових, на фоні глюкокортикоїдної терапії, що не корелює із клінічною симптоматикою захворювання та активністю хвороби, має насторожити практичних лікарів щодо виникнення асептичних некрозів кісток та слугувати обґрунтуванням необхідності проведення МРТ суглобів. Згідно з даними літератури, фактором ризику розвитку асептичних некрозів кісток є накопичення дози глюкокортикоїдів, що еквівалентна ≥2 г преднізолону, протягом 2–3 міс терапії, при цьому ризик виникнення остеонекрозу особливо високий у період від 2-го до 3-го місяця. Згідно з останніми даними, у приблизно 40% хворих, які лікуються глюкокортикоїдами, розвивається аваскулярний некроз кісток.
Остеонекроз — ураження різних відділів кістки множинної етіології, що виникає у відповідь на порушення в ній кровообігу і призводить до загибелі кісткового мозку і трабекулярної кістки [3]. Найчастіше під остеонекрозом розуміють ураження субхондральних відділів кістки, проте остеонекроз може зачіпати різні відділи. Зазвичай остеонекрози поділяють на 4 види [2]:
1. Ішемічний остеонекроз (асептичний, аваскулярний), що розвивається у відповідь на припинення судинного харчування кістки при тромбозі судин.
2. Остеонекроз, що виникає внаслідок патологічних змін, пов’язаних із набряком кісткового мозку або субхондральних відділів кістки, частіше асоціюється із хронічним артритом, артрозом, локальним і генералізованим остеопорозом.
3. Остеонекроз щелепи, пов’язаний із тривалим застосуванням бісфосфонатів у лікуванні при кісткових метастазах у пацієнтів онкологічного профілю.
4. Спорадичний остеонекроз (хвороба Легга — Кальве — Пертеса, хвороба Осгуда — Шлаттера, хвороба Келера, хвороба Хаглунда — Шинца та ін.).
Водночас незалежно від причин, що призводять до остеонекрозу, низка механізмів є спільною для всіх його типів, як і кінцевою точкою для всіх типів остеонекрозу є апоптоз остеобластів і остеоцитів [14]. Наприклад, і асептичний некроз, і остеонекроз субхондральних відділів кісток у навантажувальних зонах при різних артритах — результат порушення харчування кісткової тканини через дефіцит судинного забезпечення. Однак рівень судинного ураження при цих формах різний. При асептичному некрозі відбувається тромбоз основної судини або її гілок, що живлять кістку. При остеонекрозі другого типу також спостерігається набряк (стиснення) мікросудинного русла, однак він має реактивний характер і є результатом порушення диференціації стромальних клітин і неадекватного поширення жирової тканини, що може механічно стискати мікросудинне русло кістки. Це може відбуватися і в разі мікропереломів кісткових балок при остеопорозі.
При асептичному некрозі остеоцити і клітини кісткового мозку гинуть внаслідок інфаркту кістки, особливо швидко в разі відсутності додаткових судинних колатералей. Оскільки колатеральне кровопостачання кістки лімітоване, то кровотік зазвичай є недостатнім [6]. Захворювання найчастіше відзначають у чоловіків (8:1) молодого і середнього віку (>⅔ усіх випадків) і становить 1,5–2% усієї ортопедичної патології [5]. Найчастішою причиною нетравматичного асептичного некрозу головки стегнової кістки є глюкокортикоїдна терапія і зловживання алкоголем [1, 14]. Основним поясненням розвитку асептичного некрозу при цих найчастіших причинах є виникнення мультифакторних порушень, що полягає у зміні жирового метаболізму з венозним стазом, гіперкоагуляцією, пошкодженням ендотелію вільними жирними кислотами і жировою емболією. Венозний стаз підвищує внутрішньокістковий тиск, утруднює потік артеріальної крові, що призводить до інфаркту кістки [8].
З причинних факторів найчіткіший зв’язок із розвитком асептичних некрозів кісток виявляє терапія глюкокортикоїдами (ГК). Остеонекроз — одне з серйозних ускладнень лікування цими високоефективними лікарськими засобами, які продовжують займати гідне місце серед сучасних фармакологічних препаратів, що широко застосовуються в ревматологічній практиці [5]. Розвиток остеонекрозу при системному червоному вовчаку, дермато-/поліміозиті, системному васкуліті пов’язаний із тривалим застосуванням ГК у супресивних дозах. За даними Т. Yoshida та співавторів, двобічне ураження великих суглобів відзначали у 90% хворих на системний червоний вовчак, які перебували на стероїдній терапії, за період від 12 до 95 міс (у середньому — через 51 міс) [15]. За останніми даними, приблизно у 40% хворих, які лікуються ГК, розвиваються аваскулярні некрози кісток [4].
До повного пояснення механізмів остеонекрозу, що розвинувся при застосуванні ГК, поки далеко, однак надається значення синергізму ефекту прямих і непрямих впливів ГК на різні клітини [13]. Інгібування канонічного Wnt-сигнального шляху внаслідок застосування ГК і стимулювання білка DKK-1 [11] може відігравати особливу роль у розвитку асептичного некрозу. Відомо, що ГК здійснюють вплив шляхом порушення балансу між диференціацією в остеогенних і адипогенних лініях клітин:
- інгібують остеобласти in vivo шляхом індукції апоптозу;
- спричинюють порушення регуляції та посилення експресії адипогенних генів (особливо PPAR-γ);
- порушують регуляцію та зменшують експресію остеогенних ліній, особливо Runx-2/Cbfal.
Іншим ключовим чинником розвитку остеонекрозу при застосуванні ГК є пригнічення регенераторної здатності кістки. Остеобласти й остеокласти, що походять із клітин — попередників гемопоезу моноцит-макрофагальних ліній, — переважні клітини — учасники резорбції кістки. У здоровій кістці відбувається скоординована і збалансована диференціація клітин — попередників зі стовбурових клітин. ГК можуть пригнічувати формування кістки за рахунок пошкодження диференціації остеобластів. ГК також стимулюють апоптоз остеобластів і остеоцитів, активізуючи каспазу-3 [3]. Добре відомий також непрямий ефект ГК — зменшення кишкової абсорбції кальцію та збільшення його ниркової екскреції.
У певних випадках асептичний некроз кісток розвивається рано, на самому початку прийому ГК, хоча симптоми захворювання можуть маніфестувати і в більш віддалені періоди хвороби. На думку М. Mont і співавторів [10], аваскулярний некроз розвивається при накопиченні дози ГК, еквівалентної ≥2 г преднізолону, протягом 2–3 міс лікування, при цьому ризик виникнення цього ускладнення особливо високий у період від 2 до 3 міс. Водночас у дослідженнях S. Inoue та співавторів [7] показано відсутність зв’язку між кумулятивною дозою ГК і розвитком асептичного некрозу. К. Ono та співавтори (1992) продемонстрували, що терапія таблетованими формами преднізолону в дозі від 30 мг/добу протягом ≥1 міс є самостійним фактором ризику розвитку асептичного некрозу кісток [12]. Однак у ряді досліджень встановлено, що у групі ризику знаходяться і хворі, які отримують курси пульс-терапії ГК. Це має велике значення, оскільки більшість пацієнтів із ревматичними захворюваннями отримують курси пульс-терапії, а не тривалі пероральні курси [9]. Отже, чинником ризику розвитку асептичного некрозу кісток може бути висока кумулятивна доза ГК (пероральних чи парентеральних), особливо на початку лікування.
Представляємо клінічний випадок розвитку множинного асептичного некрозу кісток у пацієнта молодого віку із дерматоміозитом.
На консультативний прийом до ревматолога звернувся пацієнт С., 23 роки, зі скаргами на появу вираженої м’язової слабкості та болю у проксимальних групах верхніх і нижніх кінцівок, що виникли у вересні 2014 р. і відтоді поступово прогресували, на біль у суглобах кистей рук, колінних суглобах без їх припухання та почервоніння, появу висипань на шкірі обличчя, долонях, грудях, на слабкість, тахікардію, задишку, підвищену втомлюваність, періодичну субфебрильну температуру тіла. Вважає себе хворим останні 3 міс, коли виникли і поступово наростали зазначені скарги.
При огляді: адекватного відживлення. Продуктивному контакту доступний. Реєструються різноманітні висипи на шкірі: еритема грудей, значна еритема долоней з максимальним пофарбуванням кінців пальців, почервоніння кутикули та принігтьових валиків, наявність папульозних висипів (деякі із виразкуванням) над п’ястково-фаланговими суглобами кистей (плями Готтрона). Навколо очей, на повіках визначається еритема з бузковим відтінком, лущення шкіри цих ділянок. Наявні поодинокі папульозні елементи на обличчі, шкірі грудей та спини. Livedo retiсularis на шкірі рук та стегон. М’язи симетричні, м’язова сила в кінцівках знижена, утім голову утримує. Відчуття дискомфорту при ковтанні. Відзначається швидке втомлення м’язів при однотипній роботі. Очі заплющує, щоки надуває правильно й достатньо. Тест 10 підйомів зі стільця — 35 с. Швидке втомлення при підйомі/спуску зі сходів, потребує додаткової опори. При пальпації м’язів відзначається незначна болючість. Екскурсія легень знижена. Аускультативно везикулярне дихання, із фокусами ослаблення дихання в нижніх відділах з обох боків. Частота дихання — 17/хв. Межі серця незначно розширені вліво. Серцеві тони ритмічні, звучність знижена, прискорені. Систолічний шум на верхівці, акцент ІІ тону на легеневій артерії. Частота серцевого дихання — 86 уд./хв. АТ — 110/70 мм рт. ст. Живіт бере участь в акті дихання. Пальпація м’язів живота безболісна. Печінка по краю реберної дуги, селезінка не досягається. Набряки на нижніх кінцівках відсутні. Сечовиділення вільне безболісне.
У загальному аналізі крові — тромбоцитопенія та підвищення швидкості осідання еритроцитів (ШОЕ) (таблиця). Визначається суттєве підвищення міозитспецифічних ферментів: креатинфосфокіназа (КФК) (тричі з перервою на 2 дні) 841 од./л, 806 од./л, 637 од./л, МВ-КФК — 19 та 7%, аланінамінотрансфераза (АлАТ) 86 од./л, аспартатамінотрансфераза (АсАТ) 84 од./л, міоглобін — 480 мкг/л (норма — до 92 мкг/л).
Антинуклеарні антитіла негативні, антитіла до дволанцюгової ДНК негативні (проводили диференційний діагноз із системним червоним вовчаком і перехресним синдромом внаслідок тромбоцитопенії), антитіла до Jo-1 <1,0 U/mL (норма <15,0 U/mL), маркери до вірусів гепатиту В і С негативні.
| Дата | Еритроцити, 10/л | Hb, г/л | Лейкоцити ·10/л | Тромбоцити, ·10/л | Паличкоядерні, % | Сегментоядерні, % | Еозинофіли, % | Базофіли, % | Лімфоцити, % | Моноцити, % | ШОЕ, мм/год |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 15.12.2014 | 3,9 | 120 | 4,9 | 51 | 3 | 75 | 0 | 0 | 33 | 11 | 20 |
Біохімічний аналіз крові від 17.12.2014 р.: загальний білок — 66 г/л, сечовина — 4,4 ммоль/л, креатинін — 65 мкмоль/л, сечова кислота — 204 мкмоль/л, холестерин загальний — 5,6 ммоль/л, білірубін загальний — 8,8 мкмоль/л, білірубін непрямий — 8,8 мкмоль/л, АлАТ — 60 од./л, АсАТ — 52 од./л, ГГТП — 31 од./л, ЛДГ — 271 од./л, КФК — 806 од./л, МВ-КФК — 7%, залізо в сироватці крові — 13,4 мкм, кальцій загальний — 2,06 ммоль/л, кальцій іонізований — 1,1 ммоль/л, глюкоза — 5,8 ммоль/л.
Загальний аналіз сечі без відхилень. Проведено колонофіброскопію та езофагогастродуоденоскопію — без органічної патології. Спірографія: показники легеневих об’ємів та легеневої вентиляції в нормі.
Ехокардіоскопія від 17.12.2014 р. — дослідження проводили на апараті «PHILIPS IE33» з використанням датчика S5–1. Аорта та стулки аортального клапана без особливостей. Аорта 2,6 см, розкриття 2,0. Передня стулка мітрального клапана нерізко ущільнена, нерізкий її сегментарний прогин до 3 мм. Праве передсердя 3,7х4,8 см. Передньозадній розмір — 2,3 см. Ліве передсердя 3,6х5,6 см. ШПП 1,8. Індекс правого шлуночка 1,12. Індекс лівого передсердя 1,75. Індекс лівого шлуночка 2,38. Кінцевий діастолічний розмір 4,9 см. Кінцевий систолічний розмір 3,2. Кінцево-діастолічний об’єм 116 мл. Кінцево-систолічний об’єм 40 мл. Фракція викиду 65%. 5С 35%. Ударний об’єм 75 МО. Хвилинний об’єм 5,4 л/хв. Регургітація на мітральному і трикуспідальному клапанах ІІ ст., мінімально підвищений тиск на легеневій артерії ≈34 мм рт. ст. Аномальна поперечна хорда в порожнині лівого шлуночка. Витончення міжпередсердної перегородки в ділянці овального вікна без переконливих ознак шунтування. Порожнини серця не розширені. Систоло-діастолічна функція лівого шлуночка збережена.
При проведенні мультиспіральної комп’ютерної томографії (МСКТ) органів грудної клітки виявлено ознаки двобічної сегментарної пневмонії, інфільтративні зміни в S10. Ультразвукова діагностика органів черевної порожнини виявила незначну спленомегалію (селезінка розмірами 122х60 мм, паренхіма середньої ехогенності, селезінкова вена — 8 мм). Денситометрія поперекового відділу хребта дозволила діагностувати остеопенічний синдром ІІ ст.: мінеральна щільність кісткової тканини — 0,890 г/см, Z-індекс =–1,8SD.
Для верифікації діагнозу дерматоміозиту проведено магнітно-резонансну томографію (МРТ) м’язів лівого стегна та біопсію м’язового клаптя з подальшим патогістологічним дослідженням (ПГД).
МРТ м’яких тканин стегна від 16.12.2014 р.: Сигнал від практично усіх груп м’язів правого стегна, міжфасціально гіперінтенсивний на pd fs, від двоголового та чотириголового м’язів, що може свідчити про запальні зміни. Більш інтенсивний МР-сигнал відзначають порівняно з лівим стегном та від волокон m. vastus intermedius, m. vastus medialis, m. rectus femoris, m. adductor magnus. Відзначається ділянка зміненого сигналу від м’яких тканин по внутрішній поверхні за рахунок біопсії. Висновок: МР-картина може відповідати дерматоміозиту.
Преімплантаційна генетична діагностика (ПГД) м’язового клаптя стегна від 17.12.2014 р. № 22754: фрагмент скелетного м’яза з дифузним набряком ендомізія та перимізіальних м’язових волокон із дистрофією та розшаруванням міофібрил (без ознак атрофії та некрозу), наявність периваскулярних лімфо-, плазмоцитарних інфільтратів і мікроваскулітів у міксоматозно набряклій перимізіальній стромі, що з урахуванням клінічних і лабораторних даних може відповідати дебюту дерматоміозиту.
Отже, при комплексному клініко-лабораторно-інструментальному обстеженні пацієнта С. встановлено такий симптомокомплекс:
- Наявність загальних симптомів: слабкість, підвищена втомлюваність, періодично субфебрильна температура тіла.
- Шкірний синдром: геліотропна еритема навколо очей, позитивний симптом «декольте», папули Готтрона, еритема долоней, гіперемія нігтьових валиків, дигітальний васкуліт.
- Ураження суглобів: поліартралгія.
- Ураження міокарда/серця — міокардит, недостатність мітрального клапана ІІ ст., синдром тахікардії.
- Ураження судин — сітчасте ліведо.
- Ураження м’язів: слабкість проксимальних груп м’язів верхніх і нижніх кінцівок, міозит зазначених груп, дисфагія.
- Підвищення міозитспецифічних ферментів — КФК, міоглобіну та АсАТ;
- МСКТ органів грудної клітки: ознаки двобічної сегментарної пневмонії, інфільтративні зміни в S10;
- МРТ м’язів та ПГД м’язового клаптя стегна підтвердили діагноз дерматоміозиту.
На підставі даного симптомокомплексу був вперше встановлений діагноз:
Первинний дерматоміозит, підгострий перебіг, активна фаза, активність IІІ, з ураженням шкіри (еритема геліотропна, еритема грудей, плями Готтрона, ліведо), м’язів проксимальних груп верхніх і нижніх кінцівок, стравоходу, грудної клітки (міозит), суглобів (поліартралгії), серця (міокардит, серцева недостатність І ст.), легень (інфільтрати, легенева недостатність 0–І ст.), аутоімунна тромбоцитопенія. Остеопенічний синдром ІІ ст.
Зважаючи на високу активність, швидке прогресування захворювання, ураження легень та серця, молодий вік пацієнта та його бажання отримати найсучаснішу терапію, було призначено 60 мг преднізолону та ритуксимаб 500 мг довенно крапельно за схемою 0, 2-й, 28-й тижні. При оцінці через 1 міс відзначено погану переносимість ГК-терапії (сильний головний біль, панічні атаки, агресивність, зміни поведінки пацієнта, різке збільшення маси тіла, формування кушингоїдного фенотипу), а також утримання високої активності дерматоміозиту. Через 6 міс терапії активність дерматоміозиту також залишалася високою, було прийнято рішення про проведення пульс-терапії дозами 500 мг метилпреднізолону та застосування метотрексату 15 мг/тиж. Водночас проводили терапію людським імуноглобуліном. Після першого курсу пульс-терапії, старту метотрексату та терапії імуноглобулінами показники міозитспецифічних ферментів знизилися до норми, суттєво регресували шкірні прояви захворювання, зник біль у м’язах. Добова доза преднізолону була знижена до 40 мг/добу.
Через 1 тиж після проведення другого курсу пульс-терапії метилпреднізолоном раптово з’явився сильний нестерпний нічний біль у правому колінному суглобі, що не усувався звичайними нестероїдними протизапальними препаратами, а потребував застосування ненаркотичних анальгетиків. При огляді правий колінний суглоб ззовні не змінений, рухи обмежені внаслідок болю, ознак синовіту/артриту не було. Пацієнт відзначив, що раніше також відчував біль в обох колінних суглобах, але інтенсивність болю була низькою.
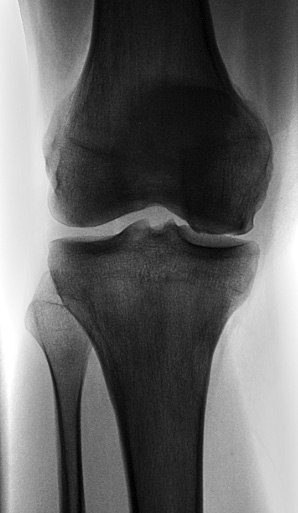
Зважаючи на високі дози ГК, використані для контролю активності захворювання, було запідозрено розвиток асептичного некрозу правого колінного суглоба. При проведенні рентгенографії правого колінного суглоба вагомих змін, що пояснили б природу інтенсивного больового синдрому, не виявлено (рис. 1). У зв’язку із триваючим болем у правому колінному суглобі було призначено МРТ цього суглоба (рис. 2–6).
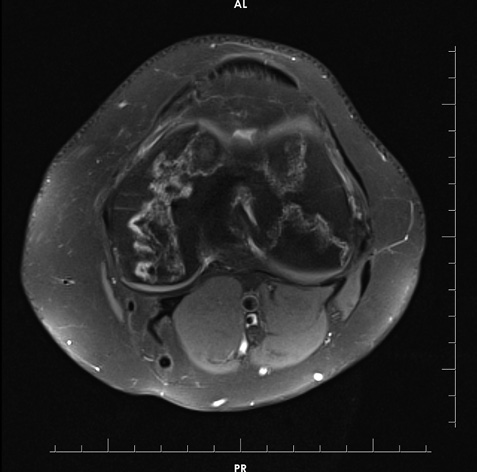
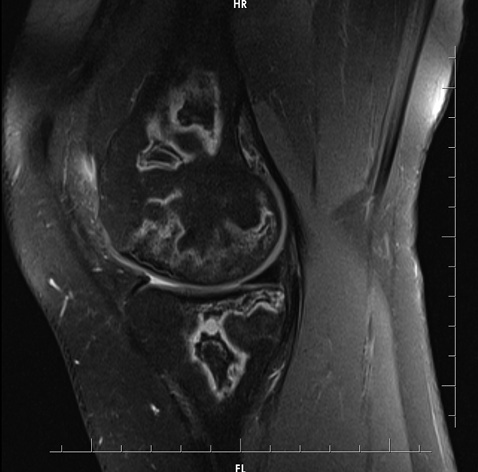
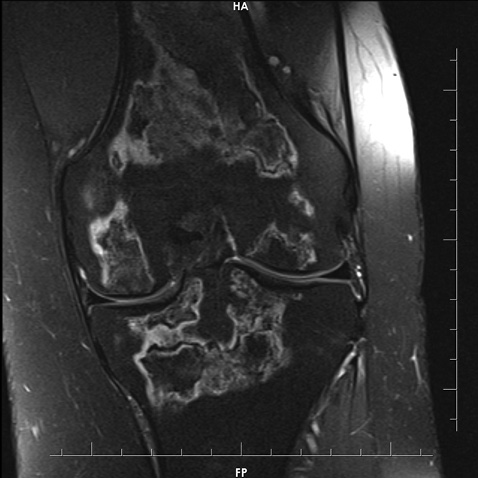
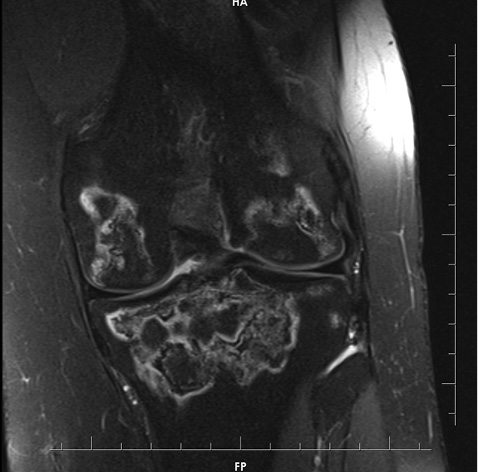
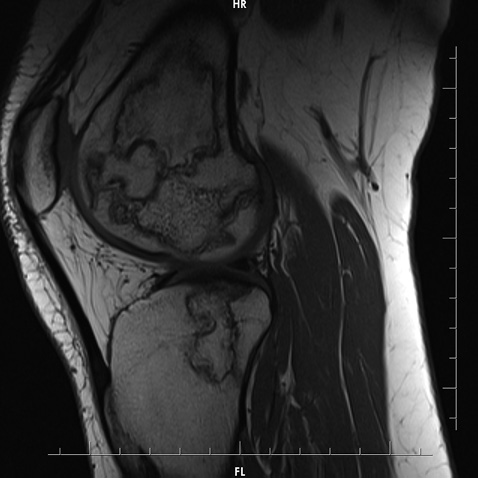
На представлених МРТ знімках правого колінного суглоба в аксіальній, сагітальній та корональній площинах, у режимах PD-WI (з придушенням МР-сигналу від жиру) та Т1–WI, у стегновій, великогомілковій кістках на рівні епіметафізів та поширюючись на діафізи кісток визначаються множинні вогнища зміненого МР-сигналу, неправильної форми, з нерівними хвилястими межами, що мають подвійний контур, ізо-/гіпоінтенсивний МР-сигнал на Т1–WI-зображеннях та гіпер-/гіпоінтенсивний на PD–WI і є лініями відмежування ділянки некрозу грануляційною тканиною з одного боку та зоною склерозу з іншого боку від незміненої кісткової тканини. У центральних відділах вогнища мають МР-сигнал, відповідний МР-сигналу від жирової тканини. Вищеописані зміни виходять на суглобові поверхні кісток, де визначається більш виражений склероз кортикального шару кісток, з ознаками ураження суглобового хряща на рівні медіального виростка правої стегнової кістки. МР-ознаки множинних інфарктів правої стегнової та великогомілкової кісток, а також надколінника.
Розвиток асептичного некрозу правого колінного суглоба було розцінено як ускладнення високодозової ГК-терапії на тлі аутоімунного захворювання. Зважаючи на біль у лівому колінному суглобі, часту симетричність асептичних некрозів суглобів, пацієнту було запропоновано проведення МРТ лівого колінного суглоба, що виявило аналогічні зміни — ознаки множинних інфарктів лівої стегнової та великогомілкової кісток.
Пацієнт проконсультований ортопедами-травматологами, а також проведено корекцію терапії: розпочато поступове зниження дози преднізолону, допризначено інфузії памідронової кислоти 60 мг довенно крапельно щомісячно, судиннотропну терапію — альпростадил 20 мкг довенно крапельно № 10. Необхідно зазначити, що з моменту встановлення діагнозу дерматоміозиту та призначення ГК пацієнт отримував комплексні препарати кальцію і вітаміну D.
Через 5 міс після цього епізоду з’явився біль у суглобах зап’ястка правої кисті значної інтенсивності без ознак артриту. Зважаючи на анамнез, пацієнту відразу було проведено МРТ правої кисті, що констатувало розвиток асептичного некрозу напівмісяцевої та човникоподібної кісток (рис. 7).
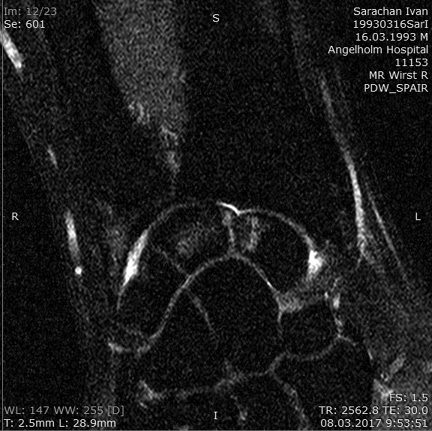
Таким чином, у пацієнта С. виявлено розвиток множинних асептичних некрозів кісток на тлі ГК-терапії. За цей період пацієнт отримував преднізолон у високих дозах від 60 мг по низхідній схемі, пульс-терапію метилпреднізолоном (сумарна доза: 2 курси по 1,5 г/міс) сумісно із базисними хворобо-модифікуючими препаратами з хорошим клінічним ефектом, що дозволило знизити активність дерматоміозиту, відновити силу м’язів, запобігти розвитку атрофії та незворотних змін м’язів, а також прогресуванню хвороби та ураженню внутрішніх органів. На момент появи симптомів асептичного некрозу колінних суглобів відзначали низьку активність дерматоміозиту.
Отже, асептичний некроз у пацієнта С. розвинувся на фоні перорального і парентерального застосування ГК у віддалені терміни (через 1 рік від дебюту захворювання та старту ГК-терапії). Можливо, у виникненні цього ускладнення відіграє роль індивідуальна чутливість до препарату та індивідуальні особливості гормонального статусу пацієнта. Водночас своєчасне застосування остеотропної та судинної терапії не дозволило запобігти розвитку подальших асептичних некрозів інших локалізацій. Таким чином, при плануванні тривалої та високодозової ГК-терапії необхідно обов’язково враховувати ймовірність розвитку асептичних некрозів кісток, у тому числі множинних, що розвиваються в різні терміни від початку застосування ГК. Поява болю у суглобах, насамперед у колінних і кульшових, що не корелює із клінічною симптоматикою захворювання та активністю хвороби, має насторожити практичних лікарів-ревматологів щодо виникнення асептичних некрозів та слугувати обґрунтуванням необхідності проведення МРТ.
Наразі пацієнт отримує 10 мг преднізолону, препарати кальцію і вітаміну D, бісфосфонати та судинну терапію. Больовий синдром купіруваний. Пацієнт готується до операції тунелізації колінних суглобів.
Список використаної літератури
- 1. Барскова В.Г., Ильиных Е.В., Смирнов А.В. и др. (2013) Остеонекроз. Часть 2. Клиника и диагностика аваскулярного некроза. Соврем. ревматол., 2: 32–36.
- 2. Башкова И.Б., Мадянов И.В. (2016) Множественные нетравматические остеонекрозы крупных суставов у молодого человека, спровоцированные непродолжительным лечением глюкокортикоидами. Русский медицинский журнал (РМЖ), 24(2): 125–128.
- 3. Ильиных Е.В., Барскова В.Г., Лидов П.И., Насонов Е.Л. (2013) Остеонекроз. Часть 1. Факторы риска и патогенез. Соврем. ревматол., 1: 17–24.
- 4. Мустафин Р.Н. (2015) Асептический некроз головки бедренной кости. Лечеб. дело, 4: 7–20.
- 5. Проценко Г.А. (2012) Асептический некроз костной ткани в ревматологии. Укр. ревматол. журн., 49(3): 52–57.
- 6. Bejar J., Peled E., Boss J.H. (2005) Vasculature deprivation — induced osteonecrosis of the rat femoral head as a model for therapeutic trials. Theor. Biol. Med. Model., 2: 24.
- 7. Inoue S., Horii M., Asano T. et al. (2003) Risk factors for nontraumatic osteonecrosis of the femoral head after renal transplantation. J. Orthop. Sci., 8: 751–756.
- 8. Jones J.P.Jr. (1997) Etiology and pathogenesis of osteonecrosis. Semin. Arthrop., 2:182–188.
- 9. Massardo L., Jacobelli S., Leissner M. et al. (1992) High dose intravenous methylprednisolone therap associated with osteonecrosis in patients with systemic lupus erythematosus. Lupus, 1(6): 401–405.
- 10. Mont M., Jones L., Hungerford D. (2006) Nontraumatic osteonecrosis of the femoral head: Ten years later. J. Bone Joint Surg. Am., 88: 1117–1132.
- 11. Ohnaka K. (2006) Wnt signaling and glucocorticoid-induced osteoporosis. Clin. Calcium., 16(11): 1812–1816.
- 12. Ono K., Tohjima T., Komazawa T. (1992) Risk factors of avascular necrosis of the femoral head in patients with systemic lupus erythematosus under high-dose corticosteroid therapy. Clin. Orthop. Relat. Res., 277: 89–97.
- 13. Tаn Gang, Kang Peng-de, Pei Fu-xing (2012) Glucocorticoids affect the metabolism of bone marrow stromal cells and lead to osteonecrosis of the femoral head: a review. Chin. Med. J., 125(1): 134–139.
- 14. Weinstein R.S., Nicholas R.W., Manolagas S.C. (2000) Apoptosis of osteocytes in glucocorticoid-induced osteonecrosis of the hip. J. Clin. Endocrinol. Metab., 85: 2907–2912.
- 15. Yoshida T., Kanayama Y., Okamura M. et al. (2002) Long-term observation of avascular necrosis of the femoral head in systemic lupus erythematosus: an MRI study. Clin. Exp. Rheumatol., 20: 525–530.
РАЗВИТИЕ МУЛЬТИФОКАЛЬНОГО АСЕПТИЧЕСКОГО ОСТЕОНЕКРОЗА У ПАЦИЕНТА С ДЕРМАТОМИОЗИТОМ КАК ОСЛОЖНЕНИЯ ГЛЮКОКОРТИКОИДНОЙ ТЕРАПИИ
Резюме. Представлено описание клинического случая развития асептического некроза коленного сустава и костей запястья у пациента с дерматомиозитом и применением глюкокортикоидов. Клинические проявления асептического некроза костей в виде интенсивного болевого синдрома развились более чем через 1 год после начала глюкокортикоидной терапии. За этот период пациент получал перорально преднизолон в стартовой дозе 60 мг/сут по нисходящей схеме и курсы пульс-терапии метилпреднизолоном (по 500 мг внутривенно капельно 3 дня подряд в месяц). Резкая, невыносимая, преимущественно ночная боль в правом коленном суставе появилась после второго курса пульс-терапии на фоне низкой активности дерматомиозита и значительного улучшения общего состояния пациента. После проведения магнитно-резонансной томографии (МРТ) правого коленного сустава верифицированы изменения, которые соответствовали инфарктам правой бедренной и большеберцовой костей. Через 4 мес после первого эпизода остеонекроза на фоне остеотропной и сосудистой терапии выявлено асептический остеонекроз костей запястья правой кисти. Появление боли в суставах, прежде всего в коленных и тазобедренных, на фоне глюкокортикоидной терапии, что не коррелирует с клинической симптоматикой заболевания и активностью болезни, должно насторожить практических врачей в плане возникновения асептических остеонекрозов и служить обоснованием проведения МРТ суставов. Согласно данным литературы, фактором риска развития асептического некроза костей является накопление дозы глюкокортикоидов, эквивалентной ≥2 г преднизолона, в течение 2–3 мес терапии, при этом риск возникновения остеонекроза особенно высок в период от 2-го до 3-го месяца. По последним данным, примерно у 40% больных, которые лечатся глюкокортикоидами, развивается аваскулярный некроз костей.
асептический остеонекроз, глюкокортикоиды, дерматомиозит, клинический случай.
Адреса для листування:
Головач Ірина Юріївна
03680, Київ, вул. Академіка Заболотного, 21
Клінічна лікарня «Феофанія» ДУС,
відділення ревматології і внутрішньої патології
E-mail: golovachirina@yandex.ru

Leave a comment