Исследование эффективности комбинации SYSADOA и влияние их применения на прием анальгетиков
Остеоартрит (ОА) — наиболее распространенное заболевание суставов, отмечающееся у 12% населения [1]. ОА представляет собой гетерогенное хроническое заболевание, поражающее все ткани сустава, включая хрящ, субхондральную кость, мениски и периартикулярные мягкие ткани [2]. К факторам риска развития ОА относят пожилой возраст, генетическую предрасположенность, ожирение, травму суставов и повышенную нагрузку на суставы [3]. В настоящее время считается, что этиология болезни включает в себя различные механические, биохимические и генетические факторы, а также молекулярные и ферментативные сигнальные каскады обратной связи, что в конечном итоге приводит к развитию и прогрессированию заболевания [4].
Медикаментозная терапия ОА включает различные лекарственные средства, которые могут быть классифицированы на основе их способа действия. Так, выделяют следующие группы препаратов: модифицирующие симптомы заболевания (симптоматические) — быстродействующие и медленнодействующие (symptomatic slow acting drugs for osteoarthritis — SYSADOA) и модифицирующие болезнь (патогенетические) [5]. К первой группе относятся симптоматические препараты быстрого действия — анальгетики (такие как парацетамол) и нестероидные противовоспалительные препараты (НПВП), которые призваны уменьшить выраженность болевого синдрома и улучшить функцию сустава. К сожалению, их применение при хронических заболеваниях ограничено короткими курсами применения в связи с развитием ряда серьезных побочных эффектов.
Вторая группа — SYSADOA — представляет собой ряд хондропротекторных препаратов, способных обеспечить уменьшение выраженности симптоматики при ОА, воздействуя на патологические механизмы развития данного заболевания, кроме того, данная группа препаратов характеризуется благоприятным профилем безопасности, что делает возможным их длительное применение. Все препараты данной группы характеризуются общей кинетикой эффективности: медленное начало, сочетающееся с сохранением эффекта препарата после его отмены [6].
К SYSADOA относятся вещества, входящие в состав хрящевой ткани (глюкозамин сульфат (ГС), хондроитин сульфат (ХС), гиалуроновая кислота, продукты расщепления коллагена) и цитокиновые модуляторы (диацереин) [7, 8], а также другие типы лекарств. Считается, что они способны отсрочить, стабилизировать или остановить патологические изменения в суставе при ОА, влияя на прогрессирование заболевания [9].
В настоящее время все более значительное место в терапии ОА занимают именно SYSАDOA. Так, в рекомендациях ESCEO (The European Society for Clinical and Economic Aspects of Osteoporosis, Osteoarthritis and Musculoskeletal Diseases — Европейское сообщество по клиническим и экономическим аспектам остеопороза и остеоартроза) 2014 г. препараты этой группы были включены в алгоритм лечения при ОА [10], поскольку наряду с симптоматическим воздействием на боль и функциональную активность пораженного сустава, они оказывают положительное влияние на метаболические процессы в хрящевой ткани и потенциально способны замедлять прогрессирование ОА (исходя из рентгеновских снимков) [11, 12]. Однако исследования этих препаратов и дискуссия по их применению продолжаются [13], что, вероятно, связано с существенными различиями в нормативном статусе, маркировке и доступности этих лекарственных средств в отдельных странах мира [14]. Поэтому при выборе того или иного препарата SYSАDOA важно ознакомиться с имеющейся доказательной базой эффективности конкретного препарата.
Эффективность применения комбинации SYSАDOA при ОА
Одним из представителей группы SYSАDOA, доступным в Украине, является комплексное средство ГЕЛАДРИНК Форте (GELADRINK Forte), которое представляет собой комбинацию широко применяемых SYSАDOA, положительные свойства которых доказаны в ходе ряда исследований. ГЕЛАДРИНК Форте содержит 3300 мг гидролизата коллагена (Gelita), 1500 мг ГС, 800 мг ХС и другие вещества (натуральный метилсульфонилметан — 600 мг, витамин С — 100 мг, витамин Е — 50 мг, селен — 50 мкг, марганец — 2 мг и экстракт босвеллии пильчатой — 100 мг). Все ключевые характеристики ГЕЛАДРИНК Форте тщательно изучены в ходе многоцентрового параллельного рандомизированного двойного слепого исследования для подтверждения эффективности данного сочетания компонентов [6]. Комбинация компонентов ГЕЛАДРИНК Форте разработана с целью сочетать в одном продукте наиболее эффективные вещества группы SYSАDOA.
Гидролизат коллагена представляет смесь пептидов коллагена с разной молекулярной массой, которые образуются посредством ферментативного расщепления коллагена, выделенного из соединительных тканей животных. Доказано, что ежедневное пероральное употребление гидролизата коллагена обладает хондропротекторным и противовоспалительным эффектами, а также антиапоптотическим действием в отношении хондроцитов сустава при ОА [8]. Следует отметить, что гидролизат коллагена обладает благоприятным профилем безопасности [15], а его положительные эффекты доказаны и в отношении костной ткани [16] и кожи [17, 18].
ГС, эндогенный аминосахарид, синтезируемый хондроцитами, является основным предшественником гликозаминогликанов, а затем аггрекана и других протеогликанов, присутствующих в хряще и являющихся частью его внеклеточного матрикса [19]. Существует несколько доступных препаратов ГС (например сульфат или гидрохлорид), продемонстрировавших различные клинические результаты, более благоприятные для ГС, чем для гидрохлорида [20]. ГС доказал свою эффективность и клиническую значимость в ряде клинических исследований [21] и в эксперименте на животных [22], продемонстрировав способность восстанавливать межклеточный матрикс хрящевой ткани, защищая хрящ от повреждений, связанных с нарушениями метаболизма межклеточного матрикса [23], и проявляя легкую противовоспалительную активность [24]. Известно, что ГС ингибирует индуцированную экспрессию гена интерлейкина-1, которая сопровождается ингибированием транскрипционного фактора NF-κB хондроцитов и синовиоцитов, что приводит к одновременному снижению синтеза циклооксигеназы-2, простагландина Е2, оксида азота (NO) и индуцированного интерлейкином-1 синтеза металлопротеиназ [25], которые, как известно, ответственны за деградацию межклеточного матрикса.
В свою очередь, ХС относится к классу природных гликозаминогликанов и представляет собой неразветвленный комплексный полисахарид, состоящий из повторяющейся дисахаридной структуры глюкуроновой кислоты и N-ацетил-D-галактозамина [26, 27]. Он является основным компонентом межклеточного матрикса, где он составляет существенный компонент протеогликанов. Его эффективность в лечении пациентов с ОА была продемонстрирована в эксперименте на животных [28], а также в клинических исследованиях [29, 30].
Известно, что потеря ХС из хрящевой ткани является элементом процесса старения на фоне ОА. Этот факт является практическим обоснованием применения экзогенного ХС. Симптоматическая эффективность ХС подтверждена результатами двух метаанализов [31, 32]. Кроме того, согласно результатам ряда исследований, применение ХС замедляет прогрессирование ОА и обладает структурно-модифицирующим воздействием [33–35].
Результаты многоцентрового параллельного рандомизированного двойного слепого исследования Геладринк Форте
В ходе исследования свойств ГЕЛАДРИНК Форте основной целью было подтверждение существования статистически достоверных различий между результатами применения данного многокомпонентного средства и плацебо путем оценки боли при ходьбе (20 м) по ВАШ во время визита Т0 (до начала лечения) и Т2 (90-й день лечения — после окончания терапии). Наряду с этим был проанализирован целый сонм терапевтических и биохимических показателей с целью изучения влияния приема SYSАDOA на состояние пациентов с ОА.
В исследовании приняли участие пациенты с ОА коленного сустава (бедренно-большеберцового сочленения) II и III стадии при наличии клинических симптомов ОА на протяжении последних 3 мес. При этом боль во время ходьбы оценивалась пациентами по шкале ВАШ ≥ 40 мм (боль при повседневной деятельности), индекс Лекена составлял ≥ 8 баллов. Возраст пациентов варьировал от 50 до 75 лет.
Таким образом, 150 пациентов были рандомизированы в пяти медицинских центрах Чехии. Разделение групп происходило в соотношении 1:1:1 (ГЕЛАДРИНК Форте/гидролизат коллагена/плацебо), при этом для статистической обработки (популяция ITT) подошли лишь 144 пациента. Парацетамол применяли в качестве средства экстренной помощи (максимальная доза — 2 г/сут).
Лечение проводили в течение 90 дней (Т2) с контрольным обследованием после 45-го дня (Т1), после чего осуществляли 30-дневное наблюдение и оценку сохранения терапевтического эффекта (эффект последействия — Т3).
Эффективность активных веществ первоначально определяли на основании оценки боли во время ходьбы по ВАШ. Вторичные параметры включали сравнение функции обследуемого сустава, пораженного ОА (оценку осуществляли по альгофункциональному индексу Лекена), оценку остаточного действия через 30 дней после завершения лечения (Т3) и применения парацетамола во время исследования. Сравнение изменений биохимических параметров (ультрачувствительный анализ на С-реактивный белок, хондрекс, пиридинолин и дезоксипиридинолин мочи) относительно исходного уровня (Т0) между лечебными группами осуществляли для объективизации оценки эффективности отдельных действующих веществ.
В соответствии с основной целью исследования, интенсивность боли при ходьбе на 20 м (ВАШ) была тщательно изучена. Было осуществлено сравнение значения сниженной интенсивности боли по ВАШ со значением, полученным до начала лечения, то есть рассчитывали разницу в интенсивности боли (РИБ). Для анализа РИБ при каждом визите (Т1, Т2, Т3) применяли критерий Уилкоксона с целью выявления статистически значимых различий между лечебными группами.
Перед началом лечения достоверных различий по исследуемым показателям между лечебными группами не отмечали. Представленность пациентов с различными стадиями ОА также была одинаковой.
Результаты исследования продемонстрировали некоторое снижение интенсивности боли на основании увеличения РИБ на момент визита T1 (45-й день). Этот показатель был сильнее выражен в группах, использовавших ГЕЛАДРИНК Форте и гидролизат коллагена, чем в группе плацебо. Различия между группами активной терапии и плацебо на момент визита Т2 (90-й день) сильнее выражены по сравнению с визитом Т1, а различие между группами, получавшими ГЕЛАДРИНК Форте и плацебо, достигает статистической достоверности (p=0,0427) (рис. 1). Для вторичного анализа была использована популяция пациентов без значимых отклонений от протокола (PPS; 123 субъекта) на момент визита T2. Средние значения РИБ для групп, получавших ГЕЛАДРИНК Форте (32 мм) и гидролизат коллагена (29 мм), были выше, чем в группе плацебо (20 мм) (рис. 2). Различия результатов между группами, получавшими ГЕЛАДРИНК Форте и плацебо, а также — между группами, принимавшими гидролизат коллагена и плацебо, были статистически достоверными.
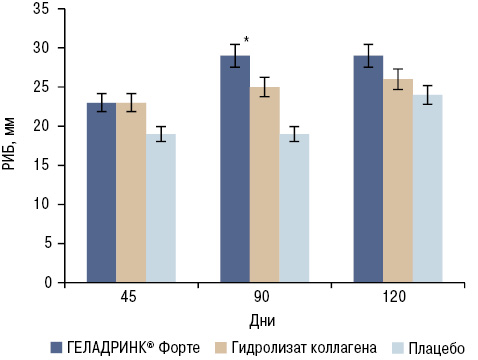
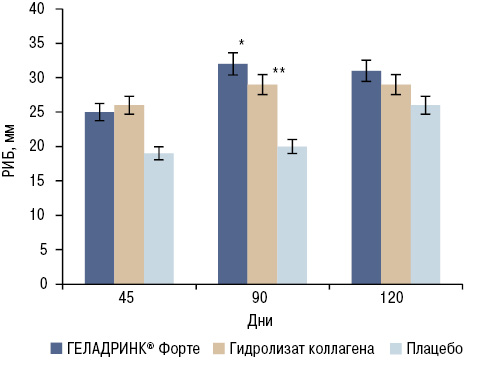
Интенсивность боли в других суставах (по ВАШ) снижалась во время приема диетической добавки и имела пограничные значения при использовании гидролизата коллагена, хотя различия между группами не были статистически достоверными. Во время исследования во всех изученных группах отмечено снижение альгофункционального индекса Лекена. Различия между отдельными группами не были статистически достоверными.
У большинства пациентов отмечали улучшение состояния (как по оценке врача, так и по собственной оценке). Улучшение в группе, получавшей ГЕЛАДРИНК Форте, было несколько более выраженным по сравнению с другими группами (68,8 и 58,3% пациентов, получавших ГЕЛАДРИНК Форте и плацебо соответственно).
Участникам исследования было разрешено применение парацетамола (препарат экстренной помощи). Пациенты использовали парацетамол в относительно небольших количествах. Тем не менее количество принятых таблеток парацетамола (1 таблетка = 500 мг) в группе, получавшей ГЕЛАДРИНК Форте, было меньше, чем в группе плацебо (18 и 31 таблетка соответственно в период Т0–Т1 и 22 и 37 таблеток соответственно в период Т1–Т2). Это свидетельствует о снижении потребности в препарате экстренной помощи на 40% в каждый из периодов наблюдения.
После проведения лечения во всех группах отмечено уменьшение концентрации пиридинолина. Оно наименее выражено в группе плацебо, а в среднем составляет –3,4 нмоль/ммоль. Статистически достоверное снижение концентрации отмечали в группе ГЕЛАДРИНК Форте по сравнению с группой плацебо (среднее снижение = –7,0 нмоль/ммоль; p=0,036). В группе, получавшей гидролизат коллагена, отмечали такой же средний показатель снижения, что и в группе, принимавшей ГЕЛАДРИНК Форте (–7,3 нмоль/ммоль). Аналогичная ситуация имела место в отношении дезоксипиридинолина. Среди пациентов, получавших ГЕЛАДРИНК Форте, отмечали более выраженное снижение концентрации дезоксипиридинолина (в среднем –1,5 нмоль/ммоль) по сравнению с группой плацебо (–0,6 нмоль/ммоль) (p=0,0174).
Таким образом, свойства и эффективность комбинации компонентов в составе ГЕЛАДРИНК Форте подтверждены в ходе исследования высокого уровня доказательности. Результаты данного многоцентрового параллельного рандомизированного двойного слепого исследования подтверждают потенциал комбинации ГС + ХС с гидролизатом коллагена. Различия значений РИБ между исследуемым продуктом и плацебо составляют приблизительно 10,0 мм, что соответствует степени эффективности в исследованиях НПВП [6]. При этом важно подчеркнуть, что применение анальгетиков снизилось на 40% среди пациентов, получавших ГЕЛАДРИНК Форте.
Список использованной литературы
- 1. Lawrence R.C., Helmick C.G., Arnett F.C. et al. (1998) Estimates of the prevalence of arthritis and selected musculoskeletal disorders in the United States. Arthr. Rheum., 41(5): 778–799.
- 2. Lawrence R.C., Felson D.T., Helmick C.G. et al. (2008) Estimates of the prevalence of arthritis and other rheumatic conditions in the United States. Part II. Arthritis Rheum., 58(1): 26–35.
- 3. Martel-Pelletier J. (2004) Pathophysiology of osteoarthritis. Osteoarthritis Cartilage, 12(Suppl A): 31–33.
- 4. Guilak F. (2011) Biomechanical factors in osteoarthritis. Best Pract. Res. Clin. Rheumatol., 25(6): 815–823.
- 5. Алексеева Л.И. (2009) Симптоматические препараты замедленного действия при лечении остеоартроза. Consilium medicus, 11(9): 100–104.
- 6. Pavelka K., Bečvář R., Böhmová J. et al. (2008) Dvojitě slepá, randomizovaná, placebem kontrolovaná, multicentrická studie ověřující účinky přípravků Geladrink Forte u pacientů s osteoartrózou kolena. Ortopedie, 2: 25–30.
- 7. Salazar J., Bello L., Chavez M. et al. (2014) Glucosamine for osteoarthritis: biological effects, clinical efficacy, and safety on glucose metabolism. Arthritis., 2014: 432–463.
- 8. Dar Q.A., Schott E.M., Catheline S.E. et al. (2017) Daily oral consumption of hydrolyzed type 1 collagen is chondroprotective and anti-inflammatory in murine posttraumatic osteoarthritis. PloS one, 12(4): e0174705.
- 9. Qvist P., Bay-Jensen A.C., Christiansen C. (2008) The disease modifying osteoarthritis drug (DMOAD): Is it in the horizon? Pharmacol. Res., 58(1): 1–7.
- 10. Bruyere O., Cooper C., Pelletier J.P. (2014) An algorithm recommendation for the management of knee osteoarthritis in Europe and internationally: A report from a task force of the European Society for Clinical and Economic Aspects of Osteoporosis and Osteoarthritis (ESCEO). Semin. Arthritis Rheum., 44(3): 253–263.
- 11. Pavelka K., Gatterovà J., Olejàrovà M. et al. (2002) Glucosamine sulphate use and delay of progression of knee OA: 3 years, randomised, placebo-controlled, double-blind study. Arch. Intern. Med., 162: 2113–2123.
- 12. Reginster J.Y., Deroisy R., Rovati L.S. et al. (2001) Long-term effects of glucosamine sulphate on osteoarthritis progression: a randomised, placebo-controlled trial. Lancet, 357: 251–256.
- 13. Яременко О.Б. (2014) Современная терапия остеоартроза на основании новых рекомендаций и доказательств: новые подходы и перспективы. Здоров’я України. Хірургія. Ортопедія. Травматологія, 2: 40–41.
- 14. Cutolo M., Berenbaum F., Hochberg M. et al. (2014) Commentary on recent therapeutic guidelines for osteoarthritis. Semin. Arthritis Rheum., 44: 611–617.
- 15. FDA. Database of Select Committee on GRAS Substances (SCGRAS) Opinion: Gelatin 1975 [updated 09/29/2015] (http://www.fda.gov/Food/IngredientsPackagingLabeling/GRAS/SCOGS/ucm261307.htm).
- 16. Guillerminet F., Beaupied H., Fabien-Soule V. et al. (2010) Hydrolyzed collagen improves bone metabolism and biomechanical parameters in ovariectomized mice: an in vitro and in vivo study. Bone., 46(3): 827–834.
- 17. Matsuda N., Koyama Y., Hosaka Y. et al. (2006) Effects of ingestion of collagen peptide on collagen fibrils and glycosaminoglycans in the dermis. J. Nutr. Sci Vitaminol. (Tokyo), 52(3): 211–215.
- 18. Asserin J., Lati E., Shioya T. et al. (2015) The effect of oral collagen peptide supplementation on skin moisture and the dermal collagen network: evidence from an ex vivo model and randomized, placebo-controlled clinical trials. J. Cosmet. Dermatol., 14(4): 291–301.
- 19. Herrero-Beaumont G.H., Rovati L.C. (2006) Use of crystaline glucosamine sulfate in osteoarthritis. Future Med., 1: 397–414.
- 20. Towheed T.E., Maxwell L., Anastassiades T.P. et al. (2005) Glucosamine therapy for treating osteoarthritis. Cochrane Database Syst. Rev., 2(2): CD002946.
- 21. Herrero-Beaumont G., Ivorra J.A., Del Carmen T.M. et al. (2007) Glucosamine sulfate in the treatment of knee osteoarthritis symptoms: a randomized, double-blind, placebo-controlled study using acetaminophen as a side comparator. Arthritis Rheum., 56(2): 555–567.
- 22. Tiraloche G., Girard C., Chouinard L. et al. (2005) Effect of oral glucosamine on cartilage degradation in a rabbit model of osteoarthritis. Arthritis Rheum., 52(4): 1118–1128.
- 23. da Camara C.C., Dowless G.V. (1998) Glucosamine sulfate for osteoarthritis. Ann. Pharmacother., 32(5): 580–587.
- 24. Shikhman A.R., Amiel D., D’Lima D. et al. (2005) Chondroprotective activity of N-acetylglucosamine in rabbits with experimental osteoarthritis. Ann. Rheum. Dis., 64(1): 89–94.
- 25. Piepoli T., Zanelli T., Letari O. et al. (2005) Glucosamine sulfate inhibits IL-1 stimulated gene expression at concentrations found in humans after oral intake. Arthritis Rheum., 52(9): 1326.
- 26. Volpi N. (2007) Analytical aspects of pharmaceutical grade chondroitin sulfates. J. Pharm. Sci., 96(12): 3168–3180.
- 27. Volpi N. (2009) Quality of different chondroitin sulfate preparations in relation to their therapeutic activity. J. Pharm .Pharmacol., 61(10): 1271–1280.
- 28. Bauerova K., Ponist S., Kuncirova V. et al. (2011) Chondroitin sulfate effect on induced arthritis in rats. Osteoarthritis Cartilage, 19(11): 1373–1379.
- 29. Hochberg M.C. (2010) Structure-modifying effects of chondroitin sulfate in knee osteoarthritis: an updated meta-analysis of randomized placebo-controlled trials of 2-year duration. Osteoarthritis Cartilage., 18(1): 28–31.
- 30. Wildi L.M., Raynauld J.P., Martel-Pelletier J. et al. (2011) Chondroitin sulphate reduces both cartilage volume loss and bone marrow lesions in knee osteoarthritis patients starting as early as 6 months after initiation of therapy: a randomised, double-blind, placebo-controlled pilot study using MRI. Ann. Rheum. Dis., 70(6): 982–989.
- 31. Leeb B.F., Schweitzen M., Montag K. et al. (2000) A meta-analysis of chondroitin sulfate in the treatment of osteoarthritis. J. Rheumatol., 27: 205–211.
- 32. McAllindon T.E., La Valley M.P., Gulin J.P. (2000) Glucosamine and chondroitin for the treatment of osteoarthritis: a systematic quality assessment and meta-analysis. JAMA, 283: 1469–1475.
- 33. Michel B., Stucki G., Frey D. et al. (2005) Chondroitins 4 and 6 sulfate in osteoarthritis of the knee. Arthritis. Rheum., 52: 779–786.
- 34. Uebelhardt D., Malaise M., Marcalongo R. et al. (2004) Intermitent treatment of knee osteoarthritis with oral chondroitin sulfate: a one year, randomized, double-blind, multicenter study versus placebo. Osteoarthritis Cart., 12: 269–276.
- 35. Moskowitz R.W. (2000) Role of collagen hydrolysate in bone and joint disease. Sem. Arthrit. Rheum., 30: 87–99.
Евгения Лукьянчук

Leave a comment