Клінічні випадки прижиттєвої діагностики ревматоїдного менінгіту з гістологічною верифікацією
- 1Клінічна лікарня «Феофанія» Державного управління справами, Київ
- 2ДЗ «Дніпропетровська медична академія» МОЗ України
Резюме. Ревматоїдний артрит (РА) — хронічне захворювання, етіологія якого остаточно не з’ясована, а у патогенезі ключову роль відіграє активація прозапальних шляхів, що призводить до суглобового й системного запалення. Якщо патологія периферичної нервової системи спостерігається доволі широко при РА, то ураження центральної нервової системи (ЦНС) виникає й діагностується значно рідше. Залучення ЦНС, як правило, розвивається у пацієнтів, які мали довгостроковий анамнез серопозитивного РА, не залежить від активності системного артриту і характеризується високим рівнем смертності, незважаючи на лікування. Оскільки клінічна симптоматика патологічного процесу, рентгенологічні ознаки, дані гістопатологічного дослідження тканин головного мозку є досить неспецифічними, діагноз ревматоїдного менінгіту (РМ) є одним із винятків. Найспецифічнішим критерієм РМ є позитивний ревматоїдний фактор у спинномозковій рідині. Наведено два клінічних спостереження прижиттєвої діагностики РМ із досить різною клінічною симптоматикою. Описано диференційний діагноз ураження ЦНС при РА з проведенням основних діагностичних процедур, надано оцінку ефективності лікування в обох випадках. Лікарі повинні бути насторожені за наявності симптомів енцефалопатії, головного болю, судом або фокального неврологічного дефіциту у пацієнтів з РА і запідозрити залучення ЦНС з призначенням відповідних досліджень, оскільки це потенційне ускладнення вимагає швидкої діагностики та специфічного лікування.
УДК 616.72-002.77:616.831.9-002]-036(048.8)
Ревматоїдний артрит (РА) є одним із найпоширеніших та найтяжчих хронічних інфекційних захворювань з високою соціальною значущістю, що пояснюється тенденцією до неухильної прогресії та високим показником інвалідизації, особливо в осіб працездатного віку [1]. РА — системне захворювання сполучної тканини з переважним ураженням дрібних суглобів за типом ерозивно-деструктивного поліартриту, але для нього характерні і різні позасуглобові прояви [5], одним із яких є ураження периферичної та центральної нервової систем (ЦНС).
Залучення ЦНС при РА — це доволі нечастий клінічний прояв, який може бути представлений васкулітом ЦНС, ревматоїдним менінгітом (РМ) з формуванням менінгеальних вузликів або без нього та дисциркуляторною енцефалопатією, специфічною до РА [3, 7, 20, 21]. Крім того, неврологічні симптоми у пацієнтів із РА можуть бути вторинними внаслідок кісткової компресії шийного відділу хребта або периферичних неврологічних структур через властивий РА атлантоаксіальний підвивих [29], компресію спинного мозку ревматоїдними вузликами [33] або внаслідок епідурального ліпоматозу [6].
РМ є рідкісним проявом РА. Неспецифічні клінічні симптоми РМ суттєво ускладнюють діагностику даного стану. За наявності менінгеальної інфільтрації симптоми можуть включати фокальний неврологічний дефіцит, судоми, дисфункцію черепних нервів або порушення свідомості [7]. Діагноз ґрунтується на поєднанні клінічних, рентгенологічних та гістологічних ознак. Швидке рішення щодо лікування є критично важливим через високий рівень смертності серед хворих на РМ. Однак жодна стандартизована схема лікування не була остаточно рекомендована, водночас є дані щодо застосування глюкокортикоїдів (ГК) та імуносупресивних препаратів. У цій роботі ми представляємо клінічні випадки РМ із різною, атиповою симптоматикою та перебігом патологічного процесу. Діагноз ґрунтувався на поєднанні клінічних, рентгенологічних та гістологічних виявів хвороби. Клінічне та рентгенологічне покращення спостерігалося після застосування високодозової пульс-терапії ГК.
Клінічне спостереження 1
70-річний чоловік з довготривалим анамнезом серопозитивного (за ревматоїдним фактором — РФ) РА (32 роки), із погано контрольованою активністю, нерегулярним прийомом хворобо-модифікуючих препаратів (DMARDs), гіпертонічною хворобою II ступеня, II стадії та гіперхолестеринемією, звернувся до лікарів швидкої допомоги з гострим правобічним геміпарезом, порушенням чутливості справа та головним болем. У приймальному відділенні лікарні швидкої допомоги лікар відзначив правобічний геміпарез із переважним ураженням нижніх кінцівок, правобічну гіперрефлексію та патологічні рефлекси справа. За шкалою DAS28 активність РА була високою (DAS28=5,4), виявлені синовіти колінних, променезап’ясткових, ліктьових, п’ястково-фалангових суглобів із множинними ерозійними змінами на рентгенограмах (ІІІ стадія РА).
Пацієнт госпіталізований до неврологічного відділення з попереднім діагнозом лівобічного ішемічного інсульту. Неврологічний дефіцит купірувався протягом ночі. Упродовж наступних днів у пацієнта спостерігалися кілька стереотипних епізодів різкої транзиторної появи правобічного геміпарезу та незначного головного болю, що тривали від 1 до 8 год. На електроенцефалограмі (ЕЕГ), яка була зроблена під час одного з таких епізодів, виявлено м’яке уповільнення та дезорганізацію тета-ритму і відсутність судомної активності. Між епізодами змін з боку неврологічного статусу не виявлено.
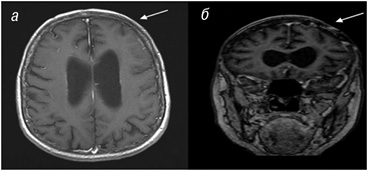
При проведенні магнітно-резонансної томографії (МРТ) головного мозку у режимі Т2-зважених зображень відмічено підвищену інтенсивність сигналу лептоменінгеальної оболонки, а також потовщення пахіменінгеальної оболонки над лівою півкулею зі збереженням структури менінгеальних оболонок, ішемічних уражень головного мозку при цьому не виявлено (рис. 1). Також не було знайдено патологічних відхилень при рентгенологічному дослідженні шийного відділу хребта.
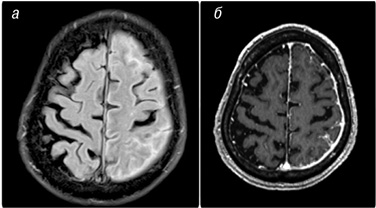
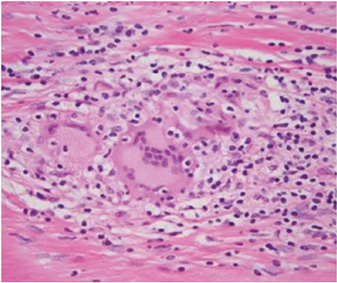
Запальні маркери у сироватці хворого були підвищеними: С-реактивний протеїн (CРП) — 7 мг/л, швидкість осідання еритроцитів (ШОЕ) — 30 мм/год, РФ — високопозитивний. Рентгенографія органів грудної порожнини, туберкуліновий тест без істотної патології. Аналіз спинномозкової рідини (СМР): незначно підвищений вміст лейкоцитів (68,0•10/л) з переважанням мононуклеарів, нормальний рівень білка (0,47 г/л) та глюкози (2,9 ммоль/л). Тести на сифіліс і криптокок були негативними. Для уточнення діагнозу та визначення нозологічної приналежності виявлених змін пацієнтові проведено стереотаксичну біопсію головного мозку; при гістологічному аналізі виявлено периваскулярну інфільтрацію запальними клітинами — B- і T-лімфоцитами; ревматоїдні вузлики були відсутніми (рис. 2).
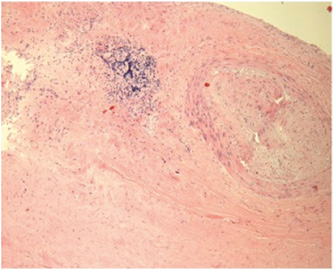
На підставі клініко-інструментальних та гістологічних даних пацієнтові встановлено діагноз РМ та призначено пульс-терапію метилпреднізолоном (МП) 1000 мг/добу довенно № 3. Згодом стан пацієнта значно поліпшився, подальших транзиторних епізодів неврологічної симптоматики не виявлялося, також суттєво регресувала суглобова активність. Пацієнт виписаний з лікарні за 14 діб. Рекомендовано прийом МП у дозі 1 мг/кг/добу з подальшим поступовим зниженням дози ГК до підтримувальної у поєднанні з комбінованою хворобо-модифікуючою терапією: гідроксихлорохін 200 мг/добу і метотрексат 15 мг/тиж. Дозу МП поступово знижували, починаючи через 1 міс від початку терапії, з досягненням 8 мг/добу через 6 міс. За цей період рецидивів ураження ЦНС не виявлено. Контрольну МРТ головного мозку проведено через 5 міс, встановлено значний регрес менінгеальних аномалій.
Клінічне спостереження 2
60-річна жінка з 23-річним анамнезом серопозитивного РА, яка останні 8 років приймала метотрексат у дозі 10–12,5 мг/тиж і МП 4–8 мг/добу, звернулася до сімейного лікаря зі скаргами на епізоди панічних атак, гострого болю у лобній частині голови, безсоння, світлобоязнь та застуду, що відзначалася через 6 днів після екстракції зуба. На комп’ютерній томограмі головного мозку змін не виявлено. Хвора проконсультована неврологом, госпіталізована до неврологічного відділення з діагнозом «панічний розлад», через 7 днів із поліпшенням виписана на амбулаторний етап. Але протягом наступних 2 тиж у пацієнтки з’явилися симптоми манії та делірію, із порушенням короткочасної пам’яті та появою зорових галюцинацій. Пацієнтка повторно проконсультована неврологом: під час огляду пацієнтка була схвильована та збуджена, не могла зосередитися. Неврологічне обстеження продемонструвало лабільний настрій, неуважність, пацієнтка «захлиналася словами», мала параноїдальні ідеї, дезорганізовані думки, погану короткочасну пам’ять, симптомів менінгізму не було, як і сенсорного або моторного дефіциту.
Під час ревматологічного огляду не виявлено ознак загострення суглобового синдрому, ревматоїдних вузликів та позасуглобових проявів РА.
У загальному аналізі крові: підвищений вміст лейкоцитів 18,6•10/л (нейтрофіли 66,5%), CРП 7 мг/л та ШОЕ 31 мм/год. Титр РФ становив >1:160, титр антитіл до циклічного цитрулінованого пептиду (аnti-ССР) був підвищений вдвічі, інші автоімунні маркери (ANA, anti-dsDNA, анті-SmDNA, анті-RNP, анті-Ro/La, антитіла до тиреоїдної пероксидази) та паранеопластична панель були у межах норми. Бактеріальні посіви крові і сечі, токсикологічні дослідження сироватки крові та сечі, тестування на ВІЛ і сифіліс були негативними. Аналіз СМР: 2 лейкоцити (лімфоцити) у полі зору, 3 еритроцити у полі зору, нормальний рівень глюкози (3,2 ммоль/л) та білка (0,4 г/л); бактеріальні, вірусні та грибкові збудники не виявлені. Комп’ютерна томографія органів грудної та черевної порожнини не виявила жодної системної аномалії. На ЕЕГ відмічено загальне уповільнення хвиль, більш виражене у лівій фронтальній ділянці. На МРТ головного мозку з контрастуванням гадолінієм зафіксовано посилення сигналу над пахіменінгеальною і лептоменінгеальною оболонками вздовж лівої фронтальної та скроневої часток, гіперінтенсивний патологічний сигнал у режимі FLAIR у суміжній паренхімальній ділянці (рис. 3).
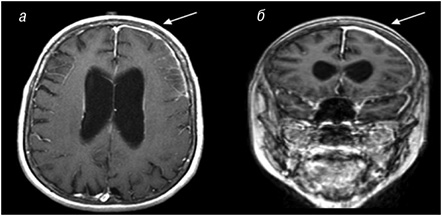
Пацієнтці встановлено попередній діагноз: вторинне ураження головного мозку органічної етіології з припущеннями про можливі інфекційні причини з огляду на недавню історію екстракції зуба, при цьому діагноз РМ вважався клінічним діагнозом виключення. Лікування було розпочато емпірично антибіотиками та противірусними препаратами (ванкоміцин, цефтріаксон, метронідазол та ацикловір). Галоперидол і вальпроєва кислота застосовувалися для поліпшення поведінкових симптомів без значного ефекту. Під час перебування хворої у стаціонарі на 5-ту добу розвинулися комплексні парціальні судомні напади, незважаючи на лікування вальпроєвою кислотою з додаванням фенітоїну. CРП зріс до 9,7 мг/л, ШОЕ — до 56 мм/год.
З огляду на показники аналізів крові, негативні дані бактеріальних/вірусних досліджень, нормальний клітинний склад і рівень білка у СМР, відсутність відповіді на антибактеріальну/противірусну терапію та відсутність ознак системної злоякісності інфекційні та неопластичні причини менінгіту вважалися малоймовірними.
У нейрохірургічному відділенні проведено стереотаксичну пункційну біопсію лобної частини лівої півкулі. Під час обстеження тверда мозкова оболонка була потовщена, жовта і покрита пухкою гранульованою тканиною; сам мозок виявився неушкодженим. Гістопатологічне дослідження виявило дифузну інфільтрацію менінгеальної оболонки лімфоцитами, гістіоцитами, плазматичними клітинами та багатоядерними гігантськими клітинами (рис. 4). Знайдено численні гранульоми з фокальним центральним некрозом. Полімеразна ланцюгова реакція до мікобактерій туберкульозу, бактеріальний аналіз на грибкові, трепонемні та кислотно-стійкі культури були негативними, тому діагноз туберкульозного або інфекційного пахіменінгіту був малоймовірним.
Встановлено діагноз гранулематозного менінгіту, вторинного до РА.
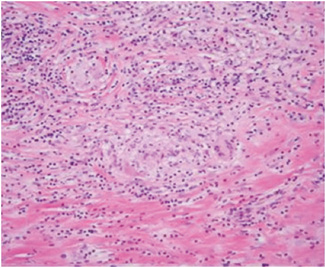
Пацієнтці призначено довенну пульс-терапію ГК (МП 1000 мг щодня протягом 3 днів), потім перехід на МП 1 мг/кг (70 мг) протягом 3 міс з поступовим зниженням до підтримувальної дози.
Після завершення курсу прийому високих доз ГК у пацієнтки відмічалося суттєве покращення з майже повним регресом симптомів захворювання, з мінімальною втратою пам’яті.
Через 1 міс у повторних аналізах крові спостерігалося зниження СРП до нормального рівня (3,6 мг/л), ШОЕ — до 35 мм/год, а через 6 тиж лікування — до 10 мм/год. Наступні контрольні МРТ-дослідження головного мозку через 3 міс продемонстрували зникнення посиленого сигналу над пахіменінгеальною та лептоменінгеальною оболонками, зменшення паренхімальної гіперінтенсивності сигналу у FLAIR-режимі (рис. 5). Поліпшення клінічних симптомів, аналізів крові та результатів МРТ надалі підтверджують встановлений діагноз РМ.
Різноманітні неврологічні симптоми є невід’ємною частиною клінічних проявів РА. У патогенетичних побудовах ураження ЦНС першорядне значення відводиться судинним змінам головного мозку. Генез цих змін пов’язаний з ішемічними ураженнями головного мозку, зумовленими запаленням судин у вигляді ексудативного васкуліту, тромбозом і тромбоемболічними ускладненнями внаслідок зниження фібринолітичної активності крові, формуванням мікрогеморагій через розрив аневризм [11, 26]. Крім того, доволі часто причиною неврологічної симптоматики у пацієнтів з РА є атлантоаксіальний підвивих, який спричинює компресію спинного мозку [29]. У цілому частота різних проявів ураження ЦНС сягає ¼ спостережень РА, причому незалежно від статі й віку пацієнтів [29]. Ризик фатальних цереброваскулярних подій удвічі перевищує аналогічний популяційний показник [11]. Ураження ЦНС у результаті ревматоїдного запального процесу може призвести, згідно з анатомічною локалізацією, до пахіменінгіту (залучення твердої мозкової оболонки) і лептоменінгіту (залучення м’якої мозкової оболонки) [7, 20, 21, 28].
Одним із найчастіших клінічних проявів ураження ЦНС при РА є РМ. За даними літератури, пацієнти з РМ мають довготривалий анамнез РА (у середньому 14 років), серопозитивний варіант захворювання, наявність численних анкілозів, як у обох наших клінічних спостереженнях, але, слід зазначити, що активний синовіт можна виявити у менш ніж половини таких клінічних випадків [31]. Це збігається з нашими клінічними спостереженнями: так, висока активність суглобового синдрому була присутня у першого пацієнта і відсутня — у другого. Дисоціацію між активністю суглобового синдрому та наявністю РМ також підкреслили численні автори [7, 23]. Одним із найчастіших клінічних проявів РМ, з яким стикаються клініцисти, є виникнення раптового, але транзиторного, нерідко персистуючого, неврологічного дефіциту. Це потребує диференціації з відомими інсультподібними станами: субдуральною гематомою, пухлиною головного мозку. Саме з таким диференційно-діагностичним завданням ми зіткнулися, особливо у першому клінічному випадку.
Слід акцентували також на інших клінічних проявах РМ, таких як: порушення психічного статусу (47%), симптоми ураження черепно-мозкових нервів (26%), геміпарези/парапарези (21%), судоми (21%), cплутаність свідомості (19%), дезорієнтація у часі та просторі (17%), фокальні короткочасні неврологічні симптоми, такі як геміплегія (16%), зорова і вестибулярна черепно-мозкова невропатії (14%) [13]. Для пахіменінгіту найтиповішими є так званий пахіменінгеальний головний біль [16] та невропатія черепно-мозкових нервів [13], спричинені запаленням або фіброзом твердої мозкової оболонки. Для лептоменінгіту більш властивими є дефіцит балансу при ході, зміна психічного стану, депресія, втрата пам’яті, судоми або парези [24]. Цікаво, що є окремі дані про маніфестації РА з ознаками ураження ЦНС, що може бути ранньою або навіть початковою ознакою ревматичного захворювання [20, 31].
Серед інструментальних методів діагностики патології нервової системи при РА найінформативнішим є МРТ. МРТ головного мозку — важливий і корисний інструмент для підтвердження діагнозу; характерними ознаками РМ є такі МРТ-симптоми: гіперсигнал в FLAIR-режимі, дифузне або локальне пахіменінгеальне та/або лептоменінгеальне контрастне посилення сигналу та потовщення оболонок. Ці ознаки вважаються патогномонічними, хоча і не цілком специфічними для РМ; трапляються випадки й нормальної картини при МРТ-дослідженні [27]. На відміну від типових проявів хронічних гранулематозних менінгеальних інфекцій, таких як туберкульоз чи саркоїдоз, посилений сигнал при РМ часто фіксується над конвекситальними борознами лобної частки, а не над основою черепа [16].
Для діагностики РМ також вельми корисним є дослідження СМР. Зазвичай при РМ при аналізі СМР показники є частіше нормальними, але можна виявити невеликий лімфоцитарний плеоцитоз та незначно підвищений рівень білка або гіпоглікемію [27]. Наявність РФ у СМР є специфічним феноменом, пов’язаним із захворюванням, і може використовуватися як біомаркер [21]. Проте у наших клінічних спостереженнях цей маркер був відсутнім, що ускладнило діагностику специфічного ураження ЦНС та спонукало до подальших діагностичних дій. Крім того, високий рівень запальних цитокінів у СМР, а саме фактора некрозу пухлини α (TNF-α), інтерлейкінів (IL)-1β і -6, відіграє центральну роль у патогенезі РА і є характерною ознакою РМ [21, 28]. Визначення цих біомаркерів не проведено нашим пацієнтам.
Остаточне підтвердження діагнозу ґрунтується на гістопатологічному аналізі менінгеальних оболонок та тканин головного мозку, який може продемонструвати 3 різні варіанти: ревматоїдні вузлики; неспецифічні ознаки менінгеального запалення, часто з периваскулярним компонентом, та наявність васкуліту [7, 23, 25]. Ревматоїдні вузлики — найпоширеніші знахідки (68%) при гістологічному дослідженні мозкової тканини у хворих на РМ, вони гістологічно ідентичні підшкірним, розташовані в черепно-мозкових оболонках (92%) і в хореоїдному сплетінні (15%) [20]. Крім того, при гістопатологічному аналізі у 63% випадків виявлено неспецифічні запальні інфільтрати в лептоменінгеальній або пахіменінгеальній оболонці мононуклеарами (здебільшого плазматичними клітинами), також можливе формування некротичних гранульом з гігантськими багатоядерними клітинами [25]. Саме за допомогою цього методу ми і встановили остаточний діагноз РМ.
Дослідження, присвячені прогнозу у таких хворих, є невеликими: смерть упродовж 4–5 міс настала у більшості хворих із РМ (84–90%), і тільки у 10–16% відмічено поліпшення клінічних та інструментальних показників [27]. Згідно з даними сучасної літератури, покращення стану хворих, швидше за все, можна отримати при використанні високодозової ГК-терапії [4]. Таке агресивне патогенетичне лікування покращує виживаність і прогноз [27, 28, 30]. При неефективності ГК рекомендується терапія циклофосфамідом [12], азатіоприном [8], циклоспорином [14] або метотрексатом [8]. Тобто імунодепресанти не завжди можуть бути необхідними на індукційній фазі лікування, показаннями до їх застосування є не тільки недосягнення бажаного ефекту лікування за допомогою ізольованого застосування ГК, а й уникання потенційних несприятливих ефектів ГК для зниження їх дози і зменшення тривалості терапії [2].
Достатньо цікавими є результати досліджень щодо застосування інгібіторів TNF-α при центральних і периферичних невропатіях. Подвійне сліпе клінічне випробування з використанням ленерцепту, розчинного димерного білка p55 TNF-IgG, показало статистично значуще збільшення кількості епізодів розсіяного склерозу порівняно з плацебо [32]. Інше проспективне дослідження продемонструвало зниження швидкості провідності на електроміографії після 12 міс терапії інфліксимабом [22]. Є кілька робіт про випадки підтвердженого біопсією асептичного аутоімунного менінгіту незабаром після ініціювання лікування інгібіторами TNF-α [9, 18, 19]. Цікавим є дослідження A. Jazeron і співавторів (2010), в якому продемонстровано рецидив неврологічних симптомів при повторному введенні адалімумабу і повне зникнення симптомів після його відміни [19]. Нещодавний ретроспективний аналіз, проведений I. Cavazzana і співавторами (2014), також ілюструє підвищення захворюваності на асептичний менінгіт у пацієнтів з РА, які отримували інгібітори TNF-α, порівняно з альтернативними синтетичними DMARDs [10]. Окрім того, є дані про рецидив РМ, що проявився переважним ураженням пахіменінгеальної оболонки, у лікованого інфліксимабом пацієнта [12], а також у пацієнта після введення адалімумабу [9, 18] та етанерцепту [15].
З теперішньою тенденцією до раннього й тривалого лікування імуномодулюючими засобами понад 2 млн пацієнтів отримували інгібітори TNF у всьому світі останні 18 років, і в нещодавньому фармакологічному огляді знайдено 772 повідомлення про неврологічні побічні ефекти, пов’язані з інгібіторами TNF-α, поданими до FDA USA у період 2000–2009 рр. [17]. Незважаючи на те що патогенез неврологічних побічних ефектів інгібіторів TNF-α є досі невідомим, лікарі повинні мати на увазі аутоімунну етіологію неврологічних симптомів у пацієнтів з терапією біологічними агентами та негайно припинити лікування у разі необхідності.
Ритуксимаб або інші моноклональні антитіла можуть мати перспективний терапевтичний ефект при РМ у майбутньому, оскільки існують дані про дієвість лікування ритуксимабом різних аутоімунних захворювань, зокрема РА.
Таким чином, РМ є надзвичайно рідкісним неврологічним ускладненням довготривалого перебігу РА. Утім, низький відсоток виявлення цього стану може бути зумовлений низькою настороженістю лікарів (сімейного лікаря, невропатолога та ревматолога) щодо специфічного ураження ЦНС у хворих на РА і непризначенням визначених методів діагностики цього ускладнення. Діагноз повинен ґрунтуватися на поєднанні клінічних, рентгенологічних та гістопатологічних особливостей. Своєчасне призначення патогенетичної терапії поліпшує прогноз захворювання і виживаність пацієнтів.
Конфлікт інтересів
Автори заявляють про відсутність конфлікту інтересів, при цьому автори не отримували від окремих осіб і організацій фінансової підтримки дослідження, гонорарів та інших форм винагород.
Інформація про внесок кожного автора
І.Ю. Головач. Концепція і дизайн дослідження, огляд літератури з проблеми, корекція тексту, підготовка статті до друку.
Є.Д. Єгудіна. Огляд літератури з проблеми, написання тексту, підготовка статті до друку.
СПИСОК ВИКОРИСТАНОЇ ЛІТЕРАТУРИ
- 1. Коваленко В.М. (2009) Ревматичні захворювання: сучасні тенденції фармакотерапії. Укр. ревматол. журн., 3(37): 5–11.
- 2. Коваленко В.Н., Головач И.Ю., Борткевич О.П. (2011) Индивидуализация лечения ревматоидного артрита: курс на достижение оптимальных результатов. Укр. ревматол. журн., 45(3): 5–15.
- 3. Синяченко О.В., Сокрут О.П., Егудина Е.Д., Сокрут В.Н. (2016) Клинико-патогенетическая значимость состояния вегетативной нервной системы при ревматоидном артрите. Междунар. неврол. журн., 85(7): 41–46.
- 4. Шуба Н.М. (2003) Сучасні підходи до лікування ревматоїдного артриту. Здоров’я України, 80: 85–91.
- 5. Яременко О.Б. (2008) Диагностика ревматоидного артрита на ранних стадиях. Здоровье Украины, 5(1): 63–65.
- 6. Arroyo I.L., Barron K.S., Brewer E.J. Jr. (1988) Spinal cord compression by epidural lipomatosis in juvenile rheumatoid arthritis. Arthr. Rheum., 31: 447–455.
- 7. Bathon J.M., Moreland L.W., DiBartolomeo A.G. (1989) Inflammatory central nervous system involvement in rheumatoid arthritis. Semin. Arthritis Rheum., 18: 258–266.
- 8. Beck D.O., Corbett J.J. (1983) Seizures due to central nervous system rheumatoid meningovasculitis. Neurology, 33(8): 1058–1061.
- 9. Booker M.J., Flint J., Saravana S. (2008) Aseptic meningitis in a patient taking etanercept for rheumatoid arthritis: a case report. Cases J., 1(1): 364–365.
- 10. Cavazzana I., Taraborelli M., Fredi M. et al. (2014) Aseptic meningitis occurring during anti-TNF-alpha therapy in rheumatoid arthritis and ankylosing spondylitis. Clin. Exp. Rheumatol., 32(5): 732–734.
- 11. Chin R.L., Latov N. (2005) Central nervous system manifestations of rheumatologic diseases. Curr. Opin. Rheumatol., 17(1): 91–99.
- 12. Chou R.C., Henson J.W., Tian D. et al. (2006) Successful treatment of rheumatoid meningitis with cyclophosphamide but not infliximab. Ann. Rheum. Dis., 65(8): 1114–1116.
- 13. Chowdhry V., Kumar N., Lachance D.H. et al. (2005) An unusual presentation of rheumatoid meningitis. J. Neuroimaging., 15: 286–288.
- 14. Claassen J., Dwyer E., Maybaum S., Elkind M.S. (2006) Rheumatoid leptomeningitis after heart transplantation. Neurology, 66(6): 948–949.
- 15. Deepak P., Stobaugh D.J., Sherid M. et al. (2013) Neurological events with tumour necrosis factor alpha inhibitors reported to the Food and Drug Administration Adverse Event Reporting System. Aliment Pharmacol. Ther., 38(4): 388–396.
- 16. Duray M.C., Marchand E., Gohy S. et al. (2012) Granulomatous meningitis due to rheumatoid arthritis. Acta Neurol. Belg., 112: 193–197.
- 17. Edwards J.C., Szczepanski L., Szechinski J. et al. (2004) Efficacy of B‐cell‐targeted therapy with rituximab in patients with rheumatoid arthritis. N. Engl. J. Med., 350(25): 72–81.
- 18. Huys A.C., Guerne P.A., Horvath J. (2012) Rheumatoid meningitis occurring during adalimumab and methotrexate treatment. Joint Bone Spine., 79(1): 90–92.
- 19. Jazeron A., Lallier J.C., Rihn B., Thiercelin M.C. (2010) Aseptic meningitis possibly induced by adalimumab. Joint Bone Spine, 77(6): 618–619.
- 20. Jones S.E., Belsley N.A., McLoud T.C. et al. (2006) Rheumatoid meningitis: radiologic and pathologic correlation. Am. J. Roentgenol., 186: 1181–1183.
- 21. Kato T., Hoshi K., Sekijima Y. et al. (2003) Rheumatoid meningitis: an autopsy report and review of the literature. Clin. Rheumatol., 22: 475–480.
- 22. Kotyla P.J., Sliwinska-Kotyla B., Kucharz E.J. (2007) Treatment with infliximab may contribute to the development of peripheral neuropathy among the patients with rheumatoid arthritis. Clin. Rheumatol., 26(9): 1595–1596.
- 23. Krysl D., Zamecnik J., Senolt L., Marusic P. (2013) Chronic repetitive nonprogressive epilepsia partialis continua due to rheumatoid meningitis. Seizure, 22: 80–82.
- 24. Kupersmith M.J., Martin V., Heller G. et al. (2004) Idiopathic hypertrophic pachymeningitis. Neurology, 62(5): 686–694.
- 25. Matsushima M., Yaguchi H., Niino M. et al. (2010) MRI and pathological findings of rheumatoid meningitis. J. Clin. Neurosci., 17: 129–132.
- 26. Sağ S., Sağ M.S., Tekeoğlu I. et al. (2017) Central nervous system involvement in rheumatoid arthritis: possible role of chronic inflammation and tnf blocker therapy. Acta. Neurol. Belg., Dec. 29. [Epub. ahead of print].
- 27. Servioli M.J., Hasiloglu Z.I., Asik M. et al. (2012) Magnetic resonance imaging of rheumatoid meningitis: a case report and literature review. Rheumatol. Int., 32: 3679–3681.
- 28. Shimada K., Matsui T., Kawakami M. et al. (2009) Diffuse chronic leptomeningitis with seropositive rheumatoid arthritis: report of a case successfully treated as rheumatoid leptomeningitis. Mod. Rheumatol., 19: 556–562.
- 29. Sofat N., Malik O., Higgens C.S. (2006) Neurological involvement in patients with rheumatic disease. Int. J. Med., 99(2): 69–79.
- 30. Spurlock R.G., Richman A.V. (1983) Rheumatoid meningitis: a case report and review of the literature. Arch. Pathol. Lab. Med., 107: 129–131.
- 31. Starosta M.A., Brandwein S.R. (2007) Clinical manifestations and treatment of rheumatoid pachymeningitis. Neurology, 68(13): 1079–1080.
- 32. The Lenercept Multiple Sclerosis Study Group and The University of British Columbia MS/MRI Analysis Group (1999) TNF neutralization in MS: results of a randomized, placebo-controlled multicenter study. Neurology, 53(3): 457–465.
- 33. Tsegaye M., Bassi S., Ashpole R.D. (2003) Extradural spinal cord compression by rheumatoid nodule. Br. J. Neurosurg., 17: 255–257.
КЛИНИЧЕСКИЕ СЛУЧАИ ПРИЖИЗНЕННОЙ ДАГНОСТИКИ РЕВМАТОИДНОГО МЕНИНГИТА С ГИСТОЛОГИЧЕСКОЙ ВЕРИФИКАЦИЕЙ
Резюме. Ревматоидный артрит (РА) — хроническое заболевание, этиология которого окончательно не выяснена, а в патогенезе ключевую роль играет активация провоспалительных путей, приводя к суставному и системному воспалению. Если патология периферической нервной системы наблюдается довольно часто при РА, то поражение центральной нервной системы (ЦНС) возникает и диагностируется значительно реже. Вовлечение ЦНС, как правило, развивается у пациентов, имеющих долгосрочный анамнез серопозитивного РА, не зависит от активности системного артрита и характеризуется высоким уровнем смертности, несмотря на лечение. Поскольку клиническая симптоматика патологического процесса, рентгенологические признаки, данные гистопатологического исследования тканей головного мозга достаточно неспецифичны, диагноз ревматоидного менингита (РМ) является одним из исключений. Наиболее специфическим критерием РМ является положительный ревматоидный фактор в спинномозговой жидкости. Представлены два клинических наблюдения РМ с весьма различной клинической симптоматикой. Описан дифференциальный диагноз поражения ЦНС при РА с проведением основных диагностических процедур, произведена оценка эффективности лечения в обоих случаях. Врачи должны быть насторожены при наличии симптомов энцефалопатии, головной боли, судорог или фокального неврологического дефицита у пациентов с РА и заподозрить вовлечение ЦНС с назначением соответствующих исследований, поскольку это потенциальное осложнение требует быстрой диагностики и специфического лечения.
ревматоидный артрит, ревматоидный менингит, поражение центральной нервной системы, биопсия, лечение.
Адреса для листування:
Головач Ірина Юріївна
03680, Київ, вул. Академіка Заболотного, 21
Клінічна лікарня «Феофанія»
Державного управління справами,
Центр ревматології
E-mail: golovachirina@gmail.com

Leave a comment