Клініко-патогенетичні аспекти псоріатичного артриту
Резюме. Подальше вивчення патогенезу псоріатичного артриту актуальне у зв’язку з недостатньою ефективністю його лікування, а отже, й пошуку нових мішеней для патогенетичної терапії. Псоріаз вважається захворюванням з переважно Т-клітинною реакцією імунної системи, а псоріатичний артрит здебільшого залучає гуморальний механізм імунної відповіді. У дослідженні підтверджена роль фактора некрозу пухлини-α як центрального цитокіну імунопатологічного процесу та хронічного запалення, яке розвивається як при псоріазі, так і при псоріатичному артриті. Але псоріатичний артрит супроводжується більш вираженою реакцією з боку В-лімфоцитів, про що свідчить як збільшення кількості самих клітин, так і підвищення рівня циркулюючих імунних комплексів та імуноглобулінів.
ВСТУП
Псоріаз — мультифакторіальне захворювання, питання його етіології залишається відкритим і нині (рис. 1).
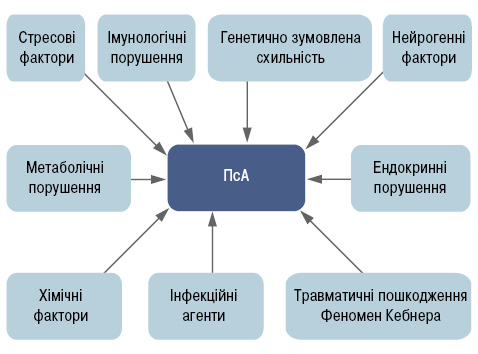
У патогенезі псоріазу суттєву роль відіграють генетичні, імунологічні, стресові, ендокринні та метаболічні фактори [1, 4, 8, 13, 14]. Певний інтерес становить поліморфізм клінічних проявів, оскільки поряд зі шкірними симптомами можливі ураження суглобів, шлунково-кишкового тракту, печінки, нирок, серцево-судинної системи та інших органів, що свідчить про системність цієї патології (табл. 1). Згідно із сучасними даними частота ПсА спостерігається у 20–30% хворих на псоріаз [15]. Суглобові прояви можуть з’являтися як після попереднього захворювання псоріазом, так і випереджати його клінічні прояви [9]. Але частота клінічних проявів ПсА суттєво вища після тривалого перебігу дерматозу, а саме від 3 до 5 років [9]. Різноманітність клінічних проявів ПсА відображена в його класифікації, згідно з класифікацією В.В. Бадокіна розрізняють клінічні форми, варіанти суглобового синдрому та наявність системних проявів (див. табл. 1) [1].
| Клінічна форма | Клініко-анатомічний варіант суставного синдрому | Системні прояви |
|---|---|---|
|
|
|
Відсутність систематизації клінічних варіантів перебігу ПсА, чіткості критеріїв активності суглобового процесу та прогнозування зумовлюють необхідність подальшого дослідження цього захворювання [7]. Для діагностики патологічних змін суглобів на ранніх етапах розвитку ПсА використовують рентгенологічні, термографічні, ультразвукові дослідження, а також магнітно-резонансну томографію, яка дозволяє визначати ураження суглобового апарату і м’яких тканин spy phone iphone free [12]. Питання щодо патогенезу уражень суглобів при псоріазі визначені не повністю, тому й зумовлюють актуальність подальшого визначення.
Мета дослідження — визначити імунологічні порушення у хворих на псоріаз на тлі вираженого суглобового синдрому, дослідити наявність кореляцій імунологічних показників і вираженості кістково-хрящових ушкоджень.
Об’єкт і методи дослідження
Обстежено 100 хворих віком від 20 до 76 років із діагнозом псоріаз та наявністю суглобового синдрому. Рентгенологічну стадію ураження суглобів визначали за Штейнброкером. Деструкцію суглобових поверхонь (0 та III стадію) виявлено у 12 % хворих, а кістковий анкілоз (IV стадію) — у 6 %. У переважної кількості хворих була наявна функціональна недостатність опорно-рухового апарату II та III ступеня. При аналізі суглобового синдрому враховували локалізацію запального процесу, симетричність ураження, наявність і вираженість ексудативного компонента в уражених суглобах і параартикулярних проявів, характер деформацій, функцію окремих суглобів та опорно-рухового апарату в цілому. Визначали вираженість больового синдрому в суглобах та хребті, наявність ранкової скутості та її тривалість, кількість уражених суглобів. Стан суглобового апарату досліджували ультразвуковим методом з використанням апарату «SONOLINE Omnia» («Siemens»), оцінювали стан кісткових суглобових поверхонь (стан кортикального шару, субхондральної кістки, наявність кіст, ерозій, інших дефектів), суглобових щілин, навколосуглобових м’яких тканин, наявність випоту, його особливості, зміни зв’язково-сухожильного апарату. Проводили загальний аналіз крові та сечі, в аналізі крові біохімічними методами визначали вміст сечовини, С-реактивного протеїну, ревматоїдного фактора. Імуноферментним методом досліджували рівні інтерлейкіну (ІЛ)-1β, ІЛ-6, ІЛ-10, фактора некрозу пухлини (ФНП)-α, кількість імуноглобулінів (Ig) класів А, М, G та рівень циркулюючих імунних комплексів (ЦІК). Визначення імунного статусу проводили за імунологічними показниками: СD3, CD4, CD8, CD16, CD19 із використанням моноклональних антитіл фірми «Bioprobe BW» (Нідерланди). Облік реакції проводився на поточному цифлюориметрі фірми «Bioprobe BW» (США). Контрольну групу становили 30 здорових осіб віком від 23 до 40 років, які не мали патології печінки, суглобів, псоріазу та інших хронічних захворювань на момент обстеження. Статистичну обробку результатів досліджень проводили за допомогою пакета прикладних програм STATISTICA 6.0.
Результати та їх обговорення
Для об’єктивізації клінічної картини псоріазу використано індекс PASI (Psoriasis area severity index), який відображає площу ураження з урахуванням тяжкості перебігу захворювання [11]. Розрахунок індексу в групі хворих коливався від 2,4 до 40,8, у середньому — на рівні 20,5±1,04. Тривалість захворювання на псоріаз становила від 8 до 40 років, тоді як активність суглобових проявів спостерігалася протягом 1–15 років. У всіх хворих відзначали больові реакції з боку уражених суглобів та їх припухлість. Кількість уражених суглобів коливалася від 2 до 21. Визначення імунологічних показників показало наявність порушень, що свідчило про залученість до розвитку запальних процесів імунної системи (табл. 2).
| Показник імунітету | Контрольна група | Хворі на ПсА |
|---|---|---|
| Лейкоцити, 10 клітин/л | 6,8±0,2 | 7,3±2,3 |
| ШОЕ, мм/год | 6,2±2,9 | 20,3±2,35* |
| Гранулоцити, % | 59,5±9,8 | 62,4±2,07 |
| Лімфоцити, % | 34±5,4 | 36,71±2,14 |
| Моноцити, % | 7,1±1,2 | 6,2±1,3 |
| CD3, % | 67,34±1,2 | 55,8±1,8* |
| CD4, % | 40,39±3,4 | 37,78±2,9 |
| CD8, % | 24,71±1,9 | 22,66±1,1 |
| CD16, % | 13,4±2,7 | 21,4±1,82* |
| CD19, % | 11,2±1,8 | 17,8±2,3* |
| CD4/CD8 | 1,63±0,21 | 1,71±0,14 |
| ЦІК | 44,38±8,3 | 75,56±18,9* |
| IgA, г/л | 1,87±0,04 | 2,03±0,12 |
| IgM, г/л | 1,54±0,08 | 0,81±0,07 |
| IgG, г/л | 9,14±1,21 | 11,15±1,63 |
| ФНП-α, пг/мл | 37,4±6,13 | 67,21±4,67* |
| IФН-γ, пг/мл | 10,81±1,71 | 15,62±2,08* |
| ІЛ-1β, пг/мл | 54,13±3,21 | 79,4±11,6* |
| IЛ-6, пг/мл | 6,11±0,24 | 11,2±0,17 |
*Різниця показників вірогідна порівняно з контрольною групою (р<0,05).
ШОЕ — швидкість осідання еритроцитів; ІФН — інтерферон.
Кількість лейкоцитів у загальному аналізі крові хворих на ПсА та показники лейкоцитарної формули не iphone spy software мали вірогідної різниці з рівнями контрольної групи і не відрізнялися від загальноклінічної норми, співвідношення гранулоцитів та агранулоцитів коливалося в межах норми. Але аналіз субпопуляції лімфоцитів виявив певні зміни, а саме: порушення співвідношення між СD3 та CD19, з перевагою В-лімфоцитів. У патогенезі псоріазу центральну роль відіграють Т-лімфоцити, але в нашому дослідженні за наявності ПсА виявлено високу активність гуморальної ланки імунітету, за рахунок якої і розвиваються ЦІК. Утворення ЦІК залежить від співвідношення антитіл і антигенів та відбувається внаслідок активації специфічної імунної реакції. У звичайних умовах ЦІК знищуються системою мононуклеарних фагоцитів, тому підвищення ЦІК свідчить, з одного боку, про антигенне навантаження та відповідну реакцію, а з іншого — про недостатню ефективність елімінації імунних комплексів із організму. Зазвичай при запальній реакції організму першою ланкою захисту виступають нейтрофіли, які виявляють фагоцитарну активність та виділяють фактори активації інших лейкоцитів, серед них і мононуклеарів, які здійснюють елімінацію і пошкоджених клітин, і утворених імунних комплексів. Але, крім відповідної активації CD19 серед популяції Т-лімфоцитів виявлено підвищення рівнів CD16, а також відповідне підвищення IФН-γ, який, у свою чергу, є потужним активатором макрофагів. У патогенезі псоріазу рядом досліджень показана його Т-клітинноопосередкована природа [6, 11]. Але, ймовірно, під час поєднання псоріазу та артриту відбуваються певні зміни в активації не лише клітинної, а й гуморальної ланки імунітету. Відомо, що під час розвитку клітинної активації при псоріазі відбувається підвищення рівнів активованих Т-лімфоцитів, Т-хелперів і цитотоксичних Т-лімфоцитів [11]. Безперечно, міжклітинна кооперація, яка відбувається під час розвитку ПсА, зумовлена перш за все Т-хелперами та опосередкованою ними активацією В-лімфоцитів, макрофагів, цитотоксичних Т-лімфоцитів та Т-лімфоцитів-супресорів. Псоріаз, на тлі якого розвивається ПсА, є мультифакторіальним захворюванням, і довгостроковий період захворювання, безумовно, впливає як на стан імунної системи, так і на інші системи організму. При псоріазі з наявністю ПсА частіше спостерігається розвиток вісцеральної патології, що зумовлює перебіг захворювання та його прогноз [3, 5, 10].
Ультразвукове дослідження — один із високоінформативних методів діагностики ПсА, оскільки дозволяє вже на ранніх стадіях діагностувати наявність синовіту та ентезитів. ПсА супроводжується кістковою резорбцією, розвитком множинних ентезитів та спондилоартриту. Ентезити є характерною ознакою ПсА, часто спостерігаються на ранній стадії захворювання та супроводжуються активним запальним процесом, дактилітами, ерозивним артритом та псоріатичною оніходистрофією [2, 8, 9]. Згідно з клінічною класифікацією (Moll J., Wright V., 1976) розрізняють п’ять типів ПсА:
- I тип — симетричний ПсА, який зазвичай вражає кілька парних суглобів, може розвиватися з різною швидкістю, а у 50% пацієнтів призводить до втрати працездатності.
- II тип — асиметричний ПсА, при якому уражаються 1–3 суглоби, наприклад колінний, ліктьовий і променезап’ястковий, але при цьому не уражаються їх парні суглоби.
- III тип — ПсА з переважним ураженням дистальних міжфалангових сполук, при якому уражаються дрібні суглоби рук і ніг. Найчастіше вражаються суглоби, розташовані ближче до нігтя, також страждають і нігті.
- IV тип — cпондильоз, при якому страждає хребет, ураження може бути в будь-якому місці, часто супроводжується ураженням сполучної тканини суглобів.
- V тип — деформуючий або spy on a cheating spouse mobile phone мутилюючий артрит, досить рідкісне, але дуже тяжке захворювання, що призводить спочатку до деформації, а потім — до руйнування дрібних суглобів і втрати їх рухливості, страждають пальці рук і ніг. Ця форма може поєднуватися з ураженням крижово-клубового з’єднання і шийних хребців.
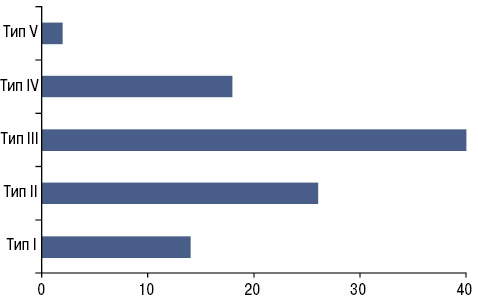
Кількісну характеристику типів ПсА у групі обстежених хворих наведено на рис. 2. У групі пацієнтів із ПсА на першому місці — ураження дистальних міжфалангових суглобів, кількість яких була на рівні майже 40%, у 26% спостерігалися асиметричні ураження, й на третьому місці — ураження хребта.
Розвиток замкненого кола при ПсА зумовлений активністю антигенпрезентуючих дендритних клітин і макрофагів, основною функцією яких є процесінг та презентація антигенів та продукція цитокінів. Підвищення рівня сигнальних молекул активує імунні клітини, які, у свою чергу, продукують нові цитокіни. Нами виявлено підвищення рівня ФНП-α на 79,7% (р<0,05), який є одним із центральних цитокінів у ланцюгу імунопатологічних реакцій при ПсА.
Тож питання етіопатогенезу ПсА залишається відкритим, оскільки поряд з імунологічними механізмами важливу роль надають генетичним факторам, таким як спадкова схильність до патології, підтвердженням якої є дані щодо наявності двох типів псоріазу, які асоційовані з генами HLA-Cw6, B13, B57, DRB1, DR7 HLA-B27 і CW2, та дослідження псоріазосприйнятливих локусів PSORS1–12, які локалізуються на різних хромосомах [14, 15].
У зв’язку з активацією гуморальної ланки імунітету у хворих на ПсА, ми вважаємо, що має місце концепція щодо наявності хронічних інфекцій та зміни реактивності пацієнта в якості стимулу імунного ураження суглобів. Надходження мікробних антигенів грампозитивних та грамнегативних мікроорганізмів можуть довгостроково зберігатися у фагосомах мононуклеарів, але з часом за певних умов викликати реактивну запальну реакцію в суглобах за феноменом Артюса [10].
Дискутується питання ролі інфекцій вірусного походження (сімейства герпес тощо) в ролі пускового механізму ПсА, оскільки зміни імунних реакцій відображають більшою мірою клітинну ланку, певний час псоріаз розглядався як «хвороба Th1» [10]. Тож, в етіопатогенезі ПсА інфекційна складова може 100 free cell phone spy software мати місце як у вигляді мікробних, так і вірусних агентів, що за умови зміненої реактивності та дисфункції імунної системи можуть стати уповільненим пусковим механізмом ланцюгової реакції.
Висновки
Одним із найважливіших механізмів у патогенезі ПсА є порушення імунної системи, але відсутність достатньої ефективності лікування зумовлює необхідність подальших досліджень цієї патології. ПсА, на відміну від псоріазу, супроводжується більш вираженою реакцією з боку В-лімфоцитів, про що свідчить підвищення як кількості самих клітин, так і рівнів ЦІК та імуноглобулінів.
список використаної Літератури
1. Бадокин В.В. (1995) К вопросу о классификации псориатической артропатии. Клин. медицина., 1: 53–57.
2. Бадокин В.В., Корсакова Ю.Л., Барсакова В.Г. и др. (2009) Терапия псориатического артрита инфликсимабом. Соврем. ревматол., 1: 29–34.
3. Беляев Г.М. (2009) Современный взгляд на проблему лечения больных псориазом. Дерматологія та венерологія. 3(45): 7–17.
4. Болевич С.Б., Уразалина А.А. (2013) Псориаз: современный взгляд на этиопатогенез. Вестн. Рос. мед. акад. наук, 2(42): 202–206.
5. Довжанский С.И. (1992) Псориаз или псориатическая болезнь. Изд-во Сарат. ун-та, Саратов. Ч.1, 96 с.
6. Коляденко К.В. (2004) Імунозалежність клінічного перебігу псоріазу: автореф. … дис. канд. мед. наук: спец. 14.01.20 Дерматологія та венерологія, Харків, 20 с.
7. Корчевская Н.Н., Артишевская Н.И. (2003) Артропатический псориаз: клиника, диагностика. Мед. новости, 12: 10–14.
8. Милевская С.Г., Пестерев П.Н. (1997) Псориатический артрит (этиология, патогенез. клиника, лечение). Сиб. мед. ун-т., Томск, 213 с.
9. Потекаев Н.Н., Серов Д.Н. (2012) Патогенетически обусловленная терапия псориаза и псориатического артрита. Клин. дерматол. и венерол., 4: 4–9.
10. Cизон О.О., Туркевич О.Ю. (2009) Патогенентичні особливості розвитку псоріатичного артриту. Укр. журн. дерматол., венерол., косметол., 2: 46–54.
11. Чернишов П.В. (2002) Субпопуляції лімфоцитів, молекули активації та адгезії на лімфоцитах периферичної крові у хворих на псоріаз. Дерматологія, 4: 6–9.
12. Янгуразова Д.Р., Арифжанов К.Р., Шакиров Є.А. (2000) Клинико-МРТ-диагностика некоторых серонегативных спондилоартритов. Тез. докл. конф. «Лучевая диагностика и лучевая терапия на пороге третьего тысячелетия», Москва, с. 705–707.
13. Ghazizadeh R., Shimizu H., Tosa M. et al. (2010) Pathogenic mechanisms shared between psoriasis and cardiovascular disease. Int. J. Med. Sci., 7(5): 284–9.
14. Han G., Williams C.A., Salter K. et al. (2010) A role for TGF-beta signaling in the pathogenesis of psoriasis. J. Invest. Dermatol.; 130(2): 371–377.
15. Villanova F., Di Meglio P., Nestle F.O. (2013) Biomarkers in psoriasis and psoriatic arthritis. Ann. Rheum. Dis., 72: 104–110.
Клинико-патогенетические аспекты псориатического Артрита
Резюме. Дальнейшее изучение патогенеза псориатического артрита является актуальным в связи с недостаточной эффективностью его лечения, а значит, и поиска новых мишеней для патогенетической терапии. Псориаз считается заболеванием с преимущественной Т-клеточной реакцией иммунной системы, а псориатический артрит в большей степени вовлекает гуморальный механизм иммунного ответа. В исследовании подтверждена роль фактора некроза опухоли-α как центрального цитокина иммунопатологического процесса и хронического воспаления, которое развивается как http://iphonespyapponline.com/ при псориазе, так и при псориатическом артрите. Но псориатический артрит сопровождается более выраженной реакцией со стороны В-лимфоцитов, о чем свидетельствует как увеличение количества самих клеток, так и повышение уровня циркулирующих иммунных комплексов и иммуноглобулинов.
псориаз, псориатический артрит, псориатическая артропатия, серонегативный спондилоартрит, провоспалительные цитокины.
Адреса для листування:
Качур Вікторія Володимирівна
03680, Київ, вул. Народного ополчення, 5
ДУ «ННЦ «Інститут кардіології
ім. М.Д. Стражеска» НАМН України»

Leave a comment