НЕРЕНТГЕНОГРАФІЧНИЙ АКСІАЛЬНИЙ СПОНДиЛОАРТРИТ: ВЕРИФІКАЦІЯ ДІАГНОЗУ ТА ЛІКУВАННЯ
Рекалов Д.Г.1, Кулинич Р.Л.1, Саржевский А.Н.2, Прыткова А.В.2, Бринер И.А.2
- 1Запорізький державний медичний університет
- 2КП «Запорожская областная клиническая больница» Запорожского областного совета
Резюме. Резюме. Одним із найважливіших кроків для ранньої діагностики та проведення раціональної, ефективної фармакотерапії вважається поява специфічної дефініції для пацієнтів зі спондилоартритом без структурних змін у клубово-крижових суглобах — нерентгенографічного аксіального спондилоартриту (Нр-АСпА). У наведеній роботі проаналізовано дані, які дозволяють чітко верифікувати захворювання на ранньому етапі, систематизувати методологічні підходи та оптимізувати терапію пацієнтів із Нр-АСпА, виходячи з результатів повномасштабних клінічних досліджень, і зокрема ABILITY-1.
Концепция спондилоартрита (СпА) последние годы базировалась на определении заболевания как состояния с преимущественным аксиальным поражением позвоночника, в то время как периферическое поражение считали ассоциированным с реактивным и псориатическим артритом (ПсА), недифференцированным СпА, а также артритом при воспалительных заболеваниях кишечника. При этом значимым в верификации диагноза считалось необходимое наличие у пациента сакроилеита в сочетании с повышенным уровнем С-реактивного белка, наличие гена гистосовместимости HLA-B27, дактилита, кожного псориаза, артрита, энтезита и/или увеита. Термин «нерентгенологический аксиальный спондилоартрит (Нр-АСпА)» был предложен Международным сообществом по лечению спондилоартритов (ASAS) в 2009 г. для максимально раннего выявления пациентов с аксиальным СпА, до выявления структурных изменений в подвздошно-крестцовых сочленениях (ПКС). Так, аксиальный СпА был разделен, согласно новой номенклатуре, на Нр-АСпА и радиографический СпА, который по своей сути является тождественным диагнозу «анкилозирующий спондилит (АС)» [12]. Весомым аргументом для имплементации новых подходов является то, что вместо дискуссии и скрупулезного выявления критериев соответствия диагнозу АС, специалисты могут сфокусировать свое внимание именно на симптомах заболевания и его максимально раннем и эффективном лечении.
Необходимым условием для верификации диагноза Нр-АСпА является наличие воспалительной боли в спине и признаки воспаления по данным магнитно-резонансной томографии (МРТ). Таким образом, особо выделяется особенность Нр-АСпА как возможно обратимого заболевания, стадии АСпА до появления рентгенологически видимых повреждений кости. Данные обсервационных исследований и результаты клинических испытаний свидетельствуют, что у пациентов с активным СпА и Нр-АСпА диагностируются сходные клинические проявления и тяжесть заболевания, требующая лечения, независимо от наличия радиографического повреждения [5, 9, 14].
Несмотря на достигнутые в последние годы успехи по ранней верификации диагноза СпА, остается актуальным вопрос своевременной и эффективной терапии, а также улучшения исходов болезни у таких пациентов. В 2013 г. во многом благодаря успешному внедрению подобных рекомендаций для лечения больных ПсА, где в ходе исследования TICOPA впервые получены данные о преимуществах подхода Т2Т над традиционным ведением пациентов [7], а также схожих результатов при курации пациентов с ревматоидным артритом [13], была сформирована рабочая группа для определения целей лечения СпА и разработки необходимых рекомендаций. Итогом работы экспертов явилась четкая программа лечения, включающая 5 общих принципов и 11 рекомендаций, имеющих своей целью достижение клинической ремиссии/низкой активности заболевания. Впервые в методологических подходах было указано на необходимость определения конкретных целей терапии и частоты мониторинга только на основании совместного решения пациента и врача.
Исходя из предложенного алгоритма Т2Т (лечение до достижения поставленной цели) при СпА (рис. 1), главной мишенью терапии является достижение устойчивой ремиссии заболевания. Критериями устойчивой ремиссии считаются достоверное снижение клинической и лабораторной активности. К сожалению, в реальной клинической практике при применении традиционных лечебных методик устойчивая ремиссия достижима в небольшой доле наблюдений, в связи с чем задачами становятся альтернативные направления, связанные с лечением пациентов исходя из функциональной активности и отсутствия позитивной лабораторно-инструментальной динамики.
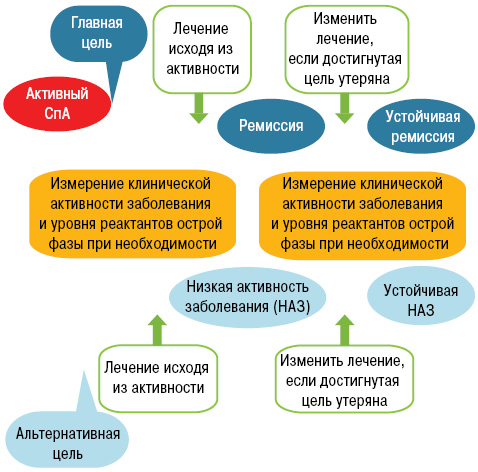
На роль удобного интегрального показателя для вышеуказанной новой стратегии, в 2009 г. van der Heijde D. и соавторами был предложен индекс активности АС (ASDAS — Ankylosing Spondylitis Disease Activity Score), который включает не только клинические, но и лабораторные значения [15]. Отличительной особенностью ASDAS является суммарная детерминация как клинических, так и лабораторных данных, в отличие от широко используемых до недавнего времени, монофункциональных показателей (BASFI — Bath Ankylosing Spondylitis Functionnal Index, BASMI — Bath Ankylosing Spondylitis Metrology Index) или суммарного индекса физической активности и тяжести СпА (BASDAI — Bath Ankylosing Spondylitis Disease Activity Index) [4]. Для определения ASDAS используют как морфофункциональные параметры, необходимые для вычисления BASDAI (1-,3-,4-й вопросы), так клинико-лабораторные значения:
- Определение боли в спине.
- Оценка общей активности заболевания пациентом.
- Выявление боли/припухлости в периферических суставах.
- Диагностика периода утренней скованности.
- Выявление повышенных значений C-реактивного белка и/или уровня скорости оседания эритроцитов (СОЭ) (по Вестергрену).
В реальной клинической практике целесообразно учитывать не только показатели активности болезни по ASDAS (<1,3 ед. — отсутствие проявлений заболевания, при показателях 1,3–2,1 ед. — низкая активность; и при уровне ≥2,1–3,5 ед. — высокая и очень высокая активность СпА соответственно), но и уровни клинического ответа. Так, считается, что о клинически значимом улучшении мы говорим при величине ∆ ≥1,1, а оценка на уровне ∆ ≥2,0 — трактуется как значительное улучшение. Возможно, именно с учетом важности определения понятий «клиническая ремиссия» и «низкая активность заболевания» при СпА — именно ASDAS следует расценивать как наиболее перспективный индекс [15].
Нестероидные противовоспалительные препараты (НПВП) считаются препаратами первой линии терапии для всех пациентов с аксиальным СпА. В то время как традиционные болезнь-модифицирующие противоревматические препараты (DMARDs), такие как метотрексат и сульфасалазин, являются недостаточно эффективными для лечения аксиального СпА [1–3, 6]. Антагонисты фактора некроза опухоли (антиФНО)-α предложены в качестве препаратов выбора для пациентов с неадекватным ответом на НПВП. Тем не менее, до недавнего времени для лечения пациентов с Нр-АСпА применение НПВП считалось безальтернативным.
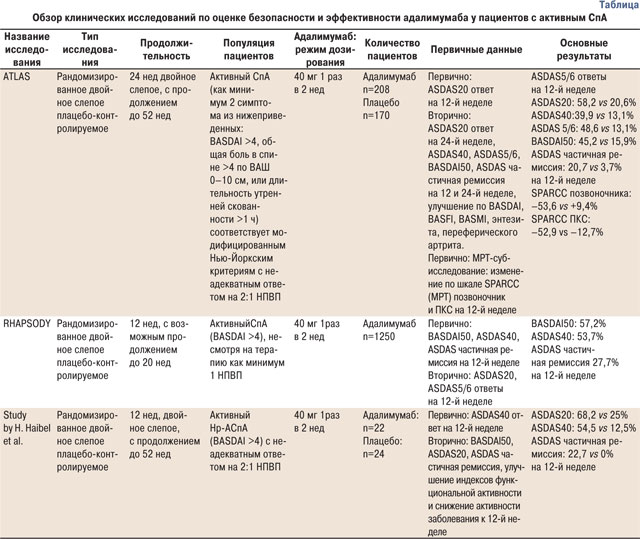
Для определения эффективности и безопасности различных схем терапии у пациентов с активным СпА был проведен целый ряд крупномасштабных клинических исследований (таблица). При этом оценивали как клинические (BASDAI, ВАШ — визуальная аналоговая шкала, ASDAS 20, 40), так и инструментальные показатели заболевания (SPARCC — Spondyloarthritis Research Consortium of Canada — МРТ-индекс, который основывается на выявлении отека костного мозга как для суставов позвоночника (диапазон значений от 0 до 108), так и для ПКС (от 0 до 72), и при значениях <2 баллов состояние пациента расценивается как ремиссия), а также интегральный показатель ASDAS [5, 11, 14]. При этом первичной задачей лечения считали достижение ASDAS частичной ремиссии на 12-й неделе при применении адалимумаба и плацебо (см. таблицу). Результаты, полученные в ходе вышеуказанных исследований, обусловили новые вопросы:
1. Эффективна ли терапия антиФНО-α для купирования клинической симптоматики и пациентов с Нр-АСпА?
2. И если да, то насколько длительно будет подавляться активность заболевания с минимальными побочными рисками?
Значимыми данными, позволяющими во многом решить прикладные задачи по лечению больных без радиографических признаков аксиального СпА, считаются результаты исследования ABILITY-1, в ходе которого оценивали эффективность и безопасность адалимумаба у пациентов с Нр-АСпА. Важной особенностью ABILITY-1 является то факт, что это первое глобальное клиническое исследование, использовавшее для классификации пациентов с Нр-АСпА критерии ASAS [11]. В клиническое исследование были включены 192 пациента в возрасте старше 18 лет с критериями неответа/непереносимости как минимум 1 НПВП и с функциональными показателями активности по BASDAI ≥4, а также болью в спине ≥40 мм по ВАШ. Критериями исключения являлись: диагноз СпА по модифицированным Нью-Йоркским критериям, наличие псориаза и ПсА и предшествующая иммунобиологическая терапия. Дизайн исследования включал слепой плацебо-контролируемый период (12 нед) с первичным анализом эффективности и период открытого приема (до 156 нед). Первичной конечной точкой являлась доля пациентов с ответом ASDAS40 на 12-й неделе, вторичными задачами были определены: ASDAS частичная ремиссия, уровень BASDAI, ASDAS-неактивное заболевание, изменения HAQ-S, а также показатели SPARCC.
При анализе результатов отмечено, что в группе больных, принимавших адалимумаб, первичной конечной точки, то есть 40% улучшения по критериям ASDAS, достигла достоверно бо`льшая часть пациентов, нежели с плацебо: 36% vs 15% (p<0,001). Что перекликается также с данными по BASDAI (50% улучшение в группе адалимумаба, а также значительное: 24 vs 4(p<0,001)), продемонстрировавшими достижение критерия неактивного заболевания (∆ ≥1,3) по ASDAS (рис. 2).
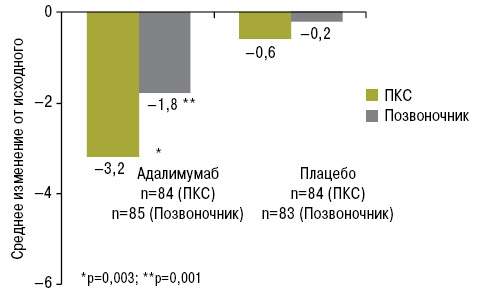
Минимально значимая разница при оценке улучшения функциональной активности по HAQ-S была получена только в группе пациентов, применявших в терапии адалимумаб [11]. При оценке структурных изменений у пациентов с Нр-АСпА при проведении ABILITY-1 использовали валидированный инструмент для оценки воспаления в суставах позвоночника и ПКС — шкалу SPARCC. При детальном анализе инструментальных данных, полученных у больных с Нр-АСпА, отмечено, что в группе адалимумаба среднее изменение значений от исходного составило –3,2 балла (р=0,003), в группе плацебо — 0,6 балла для ПКС и –1,8 балла (р=0,001) — для суставов позвоночника, в группе плацебо изменения практически отсутствовали — 0,2 балла (рис. 3).
Позитивным моментом был отмечен тот факт, что частота развития как серьезных (5 пациентов — при применении адалимумаба и 2 — плацебо), так и несерьезных нежелательных явлений (по 34 события) в группе пациентов, принимавших активное лечение и плацебо, практически сопоставима. Среди диагностированных несерьезных нежелательных явлений чаще всего отмечали инфекционные поражения, а также патологические изменения гепатобилиарной системы, что соответствует данным литературы [16].
Таким образом, результаты, полученные в крупномасштабных клинических исследованиях [8, 9, 11], являются значимым подтверждением необходимости максимально раннего и агрессивного применения терапии биологическими агентами (адалимумаб) для предотвращения развития как функциональных, так и морфологических изменений в позвоночном столбе и ПКС у обоснованно выделенной группы СпА — пациентов с Нр-АСпА.
ВЫВОДЫ
1. Термин Нр-АСпА был введен в клиническую практику для ранней диагностики пациентов с СпА, при отсутствии структурных изменений в ПКС.
2. Получены первые данные о преимуществах концепции Т2Т при ведении пациентов со Нр-АСпА, по сравнению с традиционным подходом.
3. Полученные в ходе ряда исследований данные об эффективности и безопасности предполагают, что адалимумаб может быть применен для лечения пациентов с Нр-АСпА, при неэффективности терапии НПВП.
Список использованной литературы
- 1. Chen J., Liu C., Lin J. (2006) Methotrexate for ankylosing spondylitis. Cochrane DatabaseSyst Rev., 4: CD004524.
- 2. Clegg D.O., Reda D.J., Weisman M.H. et al. (1996) Comparison of sulfasalazine and placeboin the treatment of ankylosing spondylitis. A Department of Veterans AffairsCooperative Study. Arthritis Rheum., 39: 2004–2012.
- 3. Dougados M., van der Linden S., Leirisalo-Repo M. et al. (1995) Sulfasalazine in thetreatment of spondylarthropathy // A randomized, multicenter, double-blind,placebo-controlled study. Arthritis Rheum., 38: 618–627.
-
4. Garrett S., Jenkinson T., Kennedy L.G. et al. (1994) A new approach to defining disease status in ankylosing spondylitis: the Bath Ankylosing Spondylitis Disease Activity Index.
viagra drug interactions http://plavixgeneric-uses.com/ plavix dosage cialis turnt propecia reviews http://cialisgeneric-pharmacy.com/ generic viagra buy accutane online
J. Rheumatol., 21: 2286–2291.
- 5. Haibel H., Rudwaleit M., Listing J. et al. (2008) Efficacy of adalimumab in the treatment ofaxial spondylarthritis without radiographically defined sacroiliitis: results of atwelve-week randomized, double-blind, placebo-controlled trial followed by anopen-label extension up to week fifty-two. Arthritis Rheum., 58: 1981–1991.
- 6. Irene E. van der Horst-Bruinsma (2013) Treatment of non-radiographic axial spondyloarthritis: it is only the beginning. Ann. Rheum. Dis., 72(6): 789–791.
- 7. Mease P. (2013) A View to the Future: Advances in the PsA Treatment Armamentarium: Abbreviations. Сlinical therapeutics, 25(3): 287–296.
- 8. Poddubnyy D., Rudwaleit M. (2013) Adalimumab for the treatment of ankylosing spondylitis and nonradiographic axial spondyloarthritis — a five-year update. Exp. Opin. Biologic. Ther., 13(11): 1599–1611.
- 9. Rudwaleit M., Haibel H., Baraliakos X. et al. (2009) The early disease stage in axialspondylarthritis: results from the German Spondyloarthritis Inception Cohort. Arthritis Rheum., 60: 717–727.
- 10. Rudwaleit M., Olivieri I., Kyriaki A. et al. (2009) Adalimumab is effective and well tolerated in treating patientswith ankylosing spondylitis who have advanced spinal fusion. Ann. Rheum. Dis., 68(5): 696–701.
- 11. Sieper J. et al. (2013) Efficacy and safety of adalimumab in patients with non-radiographic axial spondyloarthritis: results of a randomised placebo-controlled trial (ABILITY-1). Ann. Rheum. Dis., 72: 815–822.
- 12. Sieper J. et al. (2013) Review: Nonradiographic axial spondyloarthritis: New definition of an old disease? Arth. Rheum., 65(3): 543–551.
- 13. Smolen J. et al. (2010) Treating rheumatoid arthritis to target: recommendations of an international task force. Ann. Rheum. Dis., 69: 631–637.
- 14. van der Heijde D., Kivitz A., Schiff M.H. et al. (2006) Efficacy and safety of adalimumab in patients with ankylosing spondylitis: results of a multicenter, randomized, double-blind, placebo-controlled trial. Arthritis Rheum., 54: 2136–2146.
- 15. van Der Heijde D., Lie E., Kvien T.K. et al. (2009) ASDAS, a highly discriminatory ASAS-endorsed disease activity score in patients with ankylosing spondylitis. Ann. Rheum. Dis., 68(12): 1811–1818.
- 16. van der Heijde D., Sieper J., Maksymowych W.P. et al. (2011) 2010 Update of theinternational ASAS recommendations for the use of anti-TNF agents in patients withaxial spondyloarthritis. Ann. Rheum. Dis., 70: 905–908.
Адрес для переписки:
Рекалов Дмитрий Геннадиевич
69035, Запорожье, просп. Маяковского, 26
Запорожский государственный
медицинский университет
E-mail: direc@bigmir.net

Leave a comment