Диференційований підхід у лікуванні при гонартрозі протизапальними препаратами залежно від мінеральної щільності кісткової тканини
Резюме. З метою визначення диференційованого підходу в лікуванні при гонартрозі протизапальними препаратами залежно від мінеральної щільності кісткової тканини (МЩКТ) оцінено результати дослідження за участю 140 пацієнтів (128 жінок, 12 чоловіків) із гонартрозом ІІ–ІІІ рентгенологічної стадії за Kellgren — Lawrence. Усіх хворих на гонартроз, залежно від терапії, розподілили на чотири рівні групи по 35 пацієнтів. Пацієнти 1-ї групи приймали хондроїтин сульфат (ХС)-4,6 пташиного походження по 500 мг 2 рази на добу протягом 6 міс та німесулід у гранульованій формі 100 мг 2 рази на добу до 15 днів. Пацієнти 2-ї групи приймали ХС-4,6 по 1 г/добу протягом 6 міс та диклофенак 50 мг 3 рази на добу до 15 днів. Пацієнти 3-ї групи приймали лише німесулід 200 мг/добу до 15 днів. Пацієнти 4-ї групи приймали диклофенак 150 мг/добу до 15 днів. При вираженому больовому синдромі курс терапії нестероїдними протизапальними препаратами повторювали з інтервалом не менше 2 тиж. Через півроку від початку дослідження при ультразвуковій денситометрії виявлено негативну динаміку Т- та Z-індексу за 6 міс у стандартних відхиленнях у 3-й та 4-й групах хворих, але через 1 рік негативна динаміка відзначалася вже у хворих усіх груп, причому достовірно менша у пацієнтів 1-ї та 2-ї груп, які застосовували ХС. Через 6 міс виявлено достовірне зниження Z-індексу у хворих 4-ї групи порівняно з 3-ю групою, що свідчить про те, що втрати кісткової маси у хворих 3-ї групи були достовірно менш значущі. Таким чином, виявлено позитивний вплив ХС на МЩКТ. Відзначена висока клінічна ефективність і виражений ефект післядії ХС у пацієнтів із гонартрозом ІІ–ІІІ рентгенологічної стадії за Kellgren — Lawrence.
Вступ
Зниження якості життя хворих на остеоартроз (ОА) залишається актуальною проблемою сучасної ревматології, незважаючи на безперервне удосконалення методів діагностики та лікування. ОА — найпоширеніше захворювання суглобів, що характеризується ураженням усіх анатомічних структур суглоба, включаючи хрящ та субхондральну кістку. Відзначено, що аномальний метаболізм субхондральної кістки сприяє прогресуванню ОА (Iovu M. et al., 2008; Souich P., 2009; Richette P. et al., 2010; Arendt-Nielsen L. et al., 2011; Funck-Brentano T. et al., 2011).
ОА — найчастіше захворювання суглобів у багатьох популяціях земної кулі, яке зазвичай маніфестує у осіб віком старше 40 років. У зв’язку із проблемою старіння населення (25,6% становлять люди віком ≥55 років) ця патологія з кожним роком набуває все більшого поширення. Виявлено значно вищу поширеність ОА у жінок, особливо в постменопаузальний період, із коморбідними метаболічними станами кісткової тканини, серед них — остеопороз (ОП). І якщо донедавна такі захворювання, як ОА і ОП, вважалися взаємовиключними, то результати останніх досліджень свідчать, що зміни в субхондральній кістці у пацієнтів з ОА впливають на процес деградації хряща (Tat S.K. et al., 2009).
Виявлено, що між кістковою і хрящовою тканинами існують загальні та взаємозалежні механізми взаємодії (Richette P. et al., 2010). Встановлено зв’язок мікротравм субхондральної кістки з пошкодженням хряща. У результаті механічної компресії остеобластів субхондральної кістки підвищується продукція інтерлейкіну-6 і знижується рівень остеопротегерину (OPG). Зниження співвідношення OPG/ліганда активатора рецептора нуклеарного фактора-каппа В (OPG/RANKL) призводить до пошкодження як кістки, так і хряща. Встановлено, що зниження співвідношення OPG/RANKL значно прискорює прогресування ОА (Souich P., 2009).
В останні роки у світовій літературі з’явилися дані про те, що деякі протизапальні препарати, серед яких нестероїдні протизапальні препарати (НПЗП), симптоматичні повільнодіючі протиартрозні (symptomatic slow acting drugs for osteoarthritis — SYSADOA), можуть впливати на мінеральну щільність кісткової тканини (МЩКТ). Нещодавні дослідження показали, що хондроїтин сульфат (ХС) (Структум «Pierre Fabre Medicament») підвищує експресію OPG в остеобластах субхондральної кістки людини, що викликає підвищення співвідношення OPG/RANKL і приводить до зниження кісткової резорбції (Iovu M. et al., 2008; Souich P., 2009).
Мета дослідження — виявити вплив протизапальних препаратів (ХС, німесуліду, диклофенаку) на МЩКТ у хворих на гонартроз та визначити диференційований підхід у лікуванні при гонартрозі протизапальними препаратами залежно від МЩКТ.
Об’єкт і методи дослідження
На базі Дніпропетровської обласної консультативної поліклініки обстежено 140 хворих на гонартроз віком від 36 до 75 років (128 жінок, 12 чоловіків), у яких діагностовано ІІ–ІІІ рентгенологічну стадію за Kellgren — Lawrence. Пацієнтів залежно від терапії, що проводилася, розподілили на чотири групи по 35 осіб. Групи були ідентичними за віком і статтю, клінічними проявами захворювання (табл. 1). Пацієнти 1-ї групи приймали ХС-4,6 по 500 мг 2 рази на добу протягом 6 міс та німесулід 100 мг 2 рази на добу до 15 днів. Пацієнти 2-ї групи приймали ХС-4,6 по 1 г/добу протягом 6 міс та диклофенак 50 мг 3 рази на добу до 15 днів. Пацієнти 3-ї групи приймали німесулід 200 мг/добу до 15 днів. Пацієнти 4-ї групи приймали диклофенак 150 мг/добу до 15 днів. При вираженому больовому синдромі проведений курс терапії НПЗП повторювали з інтервалом не менше 2 тиж.
| Показник | Група | |||
|---|---|---|---|---|
| 1-ша(n=35) | 2-га(n=35) | 3-тя(n=35) | 4-та(n=35) | |
| Вік, років | 57,17±1,57 | 55,20±1,64 | 56,70±1,86 | 52,07±1,21 |
| Жінки, % | 91,4 | 94,3 | 88,6 | 91,4 |
| Чоловіки, % | 8,6 | 5,7 | 11,4 | 8,6 |
| Індекс маси тіла (ІМТ), ум. од. | 29,83±0,78 | 32,14±0,91 | 29,14±0,92 | 29,60±0,78 |
| Тривалість захворювання, років | 7,40±1,02 | 7,11±0,94 | 6,91±0,92 | 5,29±0,59 |
| Сумарний показник індексу WOMAC, мм | 965,90±201,24 | 905,70±191,91 | 979,17±191,03 | 925,27±182,39 |
| Індекс Лекена, балів | 14,73±2,59 | 14,07±2,35 | 14,90±2,43 | 14,13±2,30 |
| Рентгенологічна стадія ІІ, % | 51,4 | 48,6 | 54,3 | 65,7 |
| Рентгенологічна стадія ІІІ, % | 48,6 | 54,4 | 45,7 | 34,3 |
| МЩКТ, Т-індекс, SD | –1,37±0,23 | –1,27±0,11 | –1,34±0,10 | –1,11±0,08 |
При включенні до дослідження проводили детальне клінічне обстеження кожного пацієнта. Обов’язково враховувалися скарги хворого, наявність і вираженість больового синдрому, обмеження рухливості, обмеження у виконанні щоденної діяльності, ступінь порушення функції суглобів. З анамнезу визначали тривалість захворювання, динаміку і прогресування суглобового синдрому, терапію та її ефективність у кожного конкретного хворого, наявність побічних ефектів терапії. Критеріями включення у дослідження були: достовірність діагнозу «гонартроз» за критеріями Американської колегії ревматологів (American College of Rheumatology — ACR) та Європейської антиревматичної ліги (European League Against Rheumatism — EULAR), наявність больових відчуттів у колінному суглобі за візуальною аналоговою шкалою болю (ВАШ) ≥40 мм при ходьбі, II–ІІІ рентгенологічна стадія гонартрозу за класифікацією Kellgren — Lawrence, відсутність протипоказань до застосування НПЗП, відсутність антиостеопоротичної терапії.
Критерії виключення: тяжка травма ураженого суглоба в анамнезі, вторинний ОА, внутрішньосуглобові ін’єкції депо-кортикостероїдів або гіалуронової кислоти протягом останнього року, гіперчутливість до досліджуваного препарату, одночасне застосування інших хондропротекторів, супутні захворювання (загострення виразки шлунка та дванадцятипалої кишки, захворювання органів кровотворення, тяжкі інфекційні захворювання, печінкова, ниркова недостатність, клінічно значимі стадії серцево-легеневої недостатності), наявність злоякісних новоутворень.
Для оцінки больового синдрому у хворих використовували ВАШ. Оцінку вираженості болю та функціонального стану колінних суглобів проводили також за допомогою індексів Лекена та WOMAC. Усім пацієнтам проводили лабораторні методи дослідження, що включали визначення загальних аналізів крові та сечі, біохімічні показники крові, серед яких креатинін, трансамінази (аспартатамінотрансфераза — АсАТ, аланінамінотрансфераза — АлАТ), сечова кислота, С-реактивний протеїн (СРП). Рентгенологічне дослідження колінних суглобів виконано у стандартних проекціях до та через 12 міс від початку лікування.
Структурно-функціональний стан кісткової тканини хворих оцінювали за допомогою методу ультразвукової денситометрії п’яткової кістки з використанням приладу Achilles («LUNAR»). Стан кісткової тканини на основі даних денситометрії визначали відповідно до сучасної класифікації остеопенії та ОП (Report of a WHO Study Group, 1994). Нормальною МЩКТ вважали, якщо зміна МЩКТ у межах 1 стандартного відхилення від референтного значення (SD), одержаного в результаті виміру МЩКТ у осіб не старше 30 років — T-індекс. Зменшену кісткову масу (остеопенію) визначали при зниженні МЩКТ нижче стандартних середніх значень цього показника у осіб молодого віку на >1 SD, але <–2,5 SD (T-індекс <–1 SD, але >–2,5 SD). ОП діагностували при зниженні МЩКТ нижче референтних середніх значень цього показника у осіб молодого віку на ≥2,5 SD (T-індекс ≤–2,5 SD), тяжкий ОП — при зниженні МЩКТ на ≥2,5 SD в комбінації з ≥1 переломами кісток. Для динамічного аналізу, крім Т-критерію, використовували Z-показник.
Статистичну обробку результатів проводили на персональному комп’ютері за допомогою програм Microsoft Excel та SPSS Statistics 9.0. Усі дані обробляли статистичними методами з обчисленням середнього арифметичного кожного з наведених показників і похибки середнього. При порівнянні даних між дослідними групами для оцінки достовірності різниці застосовували коефіцієнт Стьюдента — Фішера (t) та обчислювали вірогідність помилки (р). Значимими вважали показники, в яких р<0,05. Для вивчення лінійних зв’язків між показниками застосовували кореляційний аналіз та Spearman.
Результати та їх обговорення
При дослідженні виявлено нормальну МЩКТ у 62 (44,3%), знижену — у 78 (55,7%) хворих. При цьому зниження МЩКТ до показників остеопенії визначено у 51 (36,4%), ОП — у 27 (19,3%) учасників.
Відзначено відмінності у клінічній картині гонартрозу у хворих зі зниженою МЩКТ. Так, зниження МЩКТ корелює з віком у хворих на гонартроз. Середній вік у групі хворих із нормальною МЩКТ становив 50,91±0,97 року, в той час як у групі хворих зі зниженою МЩКТ — 58,98±1,06 року. Середній рівень болю в колінних суглобах у спокої та при ходьбі за ВАШ у пацієнтів зі зниженою МЩКТ суттєво перевищував (р<0,0001) такий у пацієнтів із нормальною МЩКТ, в середньому у спокої на 19,8%, при ходьбі — на 26,7% (табл. 2).
| Рівень болюза ВАШ | Пацієнти | |
|---|---|---|
| з нормальною МЩКТ(n=62) | зі зниженою МЩКТ(n=78) | |
| У спокої, мм | 45,00±5,62 | 53,91±8,94* |
| При ходьбі, мм | 54,75±9,11 | 69,37±9,21* |
У табл. 2, 3, 5: *р<0,0001.
| Показник | Пацієнти | |
|---|---|---|
| з нормальною МЩКТ | зі зниженою МЩКТ | |
| Розділ А (біль у спокої та при рухах), мм | 194,73±21,23 | 232,65±25,99* |
| Розділ Б (обмеження рухливості), мм | 70,38±15,21 | 104,23±24,08* |
| Розділ В (обмеження у виконанні щоденної діяльності), мм | 555,58±115,50 | 709,78±133,29* |
| Сумарний показник анкети WOMAC, мм | 822,69±141,98 | 1046,66±167,17* |
| Індекс Лекена, балів | 12,89±1,89 | 15,78 ±1,98* |
Крім того, рівень болю за WOMAC у хворих зі зниженою МЩКТ (232,65±25,99 мм) також виявився значно вищим (р<0,0001), ніж у осіб з нормальною щільністю (194,73±21,23 мм), в середньому на 19,6% (табл. 3). Показник обмеженості рухливості суглоба вранці та протягом дня за WOMAC у пацієнтів зі зниженою МЩКТ (104,23±24,08 мм) був також достовірно вищим (р<0,0001), ніж у осіб з нормальною МЩКТ (70,38±15,21 мм), в середньому на 48%. Показник обмеження повсякденної активності за WOMAC у осіб зі зниженою МЩКТ (709,78±133,29 мм) був достовірно вищим, ніж у хворих на гонартроз із нормальною щільністю кістки (555,58±115,50 мм), у середньому на 27,8%. Таким чином, сумарний індекс WOMAC у осіб зі зниженою МЩКТ був достовірно вищим (у середньому на 27,2%) порівняно з особами з нормальною МЩКТ (рис. 1). Це ж стосується й індексу Лекена, який у хворих зі зниженою МЩКТ становив 15,78±1,98 бала, а з нормальною — 12,89±1,89 бала. Індекс Лекена у групі хворих зі зниженою МЩКТ був у середньому вищим на 22,4%.
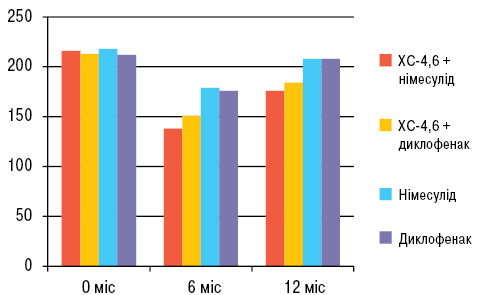
Рис. 1. Динаміка рівня болю за WOMAC
Серед обстежених переважали хворі на гонартроз II рентгенологічної стадії — 77 (55%), з них знижену щільність кісткової тканини відзначали у 39 (50,6%) осіб, нормальну — у 38 (49,4%). III рентгенологічну стадію виявили у 63 (45%) пацієнтів, з них знижену МЩКТ — у 39 (61,9%), нормальну — у 24 (38,1%) осіб. Стан кісткової тканини хворих на ОА колінних суглобів залежно від рентгенологічної стадії гонартрозу наведено в табл. 4.
| Показники МЩКТ | II рентгенологічна стадія | III рентгенологічна стадія | ||||
|---|---|---|---|---|---|---|
| Нормальна МЩКТ (n=38) | Знижена МЩКТ(n=39) | Нормальна МЩКТ (n=24) |
Знижена МЩКТ(n=39) | |||
| Оп (n=28) |
ОП (n=11) |
Оп (n=23) |
ОП (n=16) |
|||
| Т-індекс, SD | –0,17±0,07 | –2,02±0,17 | –0,23±0,08* | –2,23±0,07* | ||
| Z-індекс, SD | 1,04±0,10 | –0,88±0,30 | 1,07±0,07 | –1,04±0,3* | ||
*р<0,05. Оп — остеопенія.
Згідно з класифікацією Kellgren — Lawrence за 12 міс спостереження прогресування рентгенологічних ознак гонартрозу не зареєстровано.
Виявлено достовірні відмінності в рівнях СРП між хворими на гонартроз із нормальними та зниженими показниками МЩКТ (табл. 5). Рівень СРП був істотно вищим (р<0,0001) у пацієнтів зі зниженою МЩКТ порівняно з нормальною (6,32±1,67 і 4,74±0,75 мг/л відповідно), в середньому — на 33,3%. При цьому рівень ШОЕ в обох групах пацієнтів достовірно не відрізнявся (у групі зі зниженою МЩКТ 10,17±2,38 мм/год, у групі з нормальною МЩКТ — 9,96±2,17 мм/год).
| Лабораторні показники | Пацієнти | |
|---|---|---|
| з нормальною МЩКТ(n=62) | зі зниженою МЩКТ(n=78) | |
| СРП, мг/л | 4,74±0,75 | 6,32±1,67* |
| ШОЕ, мм/год | 9,96±2,17 | 10,17±2,38 |
У результаті проведеного кореляційного аналізу показників клінічних, лабораторних та інструментальних досліджень у пацієнтів із гонартрозом встановлено, що достовірного кореляційного зв’язку між МЩКТ й ІМТ не виявлено (r<0,3). ІМТ корелював із рівнем болю за ВАШ у спокої (r=0,562), рівнем болю за WOMAC (r=0,541), показником обмеження повсякденної активності за WOMAC (r=0,421), індексом Лекена (r=0,463) та рентгенологічною стадією ОА (r=0,393).
Виявлено зворотний середній кореляційний зв’язок між показниками МЩКТ (Т- і Z-індекси) і віком хворих (r=–0,562). Вік пацієнтів також корелював із тривалістю захворювання (r=0,954), рентгенологічною стадією гонартрозу (r=0,468), індексом Лекена (r=0,415), рівнями болю за ВАШ (r=0,418) і за WOMAC (r=0,424), показником обмеження повсякденної активності за WOMAC (r=0,533). Виявлено кореляційний зв’язок між показниками скутості суглобів і обмеження повсякденної діяльності за WOMAC та індексом Lequesne (r=0,621).
Виявлено помірний зворотний кореляційний зв’язок між показниками МЩКТ і рівнем болю за ВАШ (r=–0,431) і WOMAC (r=–0,433), показником обмеження повсякденної активності за WOMAC (r=–0,393). Також встановлено незначний зворотний кореляційний зв’язок між показниками МЩКТ та індексом Лекена (r=–0,315). Виявлено незначний зворотний кореляційний зв’язок між показниками МЩКТ та рентгенологічною стадією гонартрозу (r=–0,314) і помірний зворотний кореляційний зв’язок між показниками МЩКТ та рівнем СРП (r=–0,402).
У результаті проведеного дослідження виявлені особливості ОА колінних суглобів у пацієнтів зі зниженою МЩКТ: більш виражені больовий синдром у колінному суглобі за ВАШ в середньому у спокої на 19,8% і при ходьбі — на 26,7%, за індексом WOMAC — на 19,6% та обмеження повсякденної активності за WOMAC на 27,8%, рентгенологічні зміни і підвищений рівень СРП у середньому на 33,3%.
У проведеному дослідженні застосування препаратів усіх груп зумовило поліпшення симптомів захворювання, більш вираженого у 1-й і 2-й групах, де застосовували ХС-4,6. Анальгезивний ефект досягався у пацієнтів усіх груп на 2–4-му тижні терапії, без статистично значущих відмінностей між групами через 1 міс від початку спостереження. Вже через 3 міс спостерігався достовірно більш виражений анальгезивний ефект у 1-й і 2-й групах, де застосовували ХС-4,6 і НПЗП (німесулід або диклофенак), ніж у 3-й і 4-й групах, де застосовували німесулід або диклофенак відповідно (див. рис. 1). Так, рівень болю за шкалою WOMAC через 3 міс достовірно (р<0,0001) був нижчим у 1-й групі (163,55±26,27 мм), ніж у 3-й (204,43±24,33 мм) і 4-й (201,28±31,38 мм), і в 2-й групі (173,41±21,67 мм) порівняно з 2-ю і 4-ю групами (р<0,01). Через 6 міс від початку терапії рівень болю за шкалою WOMAC достовірно (р<0,0001) був нижчим у 1-й групі (138,53±27,24 мм), ніж у 3-й (179,57±24,06 мм) і 4-й (176,33±30,44 мм), а також у 2-й групі (173,41±21,67 мм) порівняно з 3-ю і 4-ю групами (р<0,01).
Через 12 міс від початку дослідження відзначено достовірно (р<0,005) нижчий рівень болю за шкалою WOMAC у 1-й групі (176,53±29,17 мм), ніж у 3-й (208,70±28,07 мм) і в 4-й групі (208,77±36,93 мм). Також через 12 міс відзначено більш низький рівень болю за шкалою WOMAC (р=0,024) у пацієнтів 2-ї групи (184,63±33,58 мм) порівняно із 3-ю (208,70±28,07 мм). При цьому 50% зниження показника WOMAC у хворих із нормальною МЩКТ досягнуто у 24% випадків, зі зниженою МЩКТ — лише у 11%. У результаті дослідження виявлено достовірне зниження рівня болю у пацієнтів із гонартрозом, яким призначали ХС-4,6 через 3; 6 і 12 міс від початку терапії.
Показник обмеженої рухливості суглоба за WOMAC достовірно не відрізнявся у всіх групах хворих протягом усього дослідження. Показник складнощів у виконанні повсякденної діяльності за WOMAC через 6 міс достовірно (р=0,012) знизився у 2-й групі (451,03±132,37 мм) порівняно з 3-ю групою (560,93±131,22 мм). Така ж тенденція збереглася і через 12 міс: показник складнощів у виконанні повсякденної діяльності за WOMAC у 2-й групі (537,83±148,25 мм) був достовірно нижчим (р=0,042), ніж у 3-й групі (646,43±156,18 мм).
| Період | Розділ А (Біль у спокої і при рухах) | Розділ Б (Обмеження рухливості) | Розділ В (Обмеження у виконанні щоденної діяльності) | Сумарний показник анкети WOMAC |
|---|---|---|---|---|
| 1-ша група (ХС + німесулід) | ||||
| До терапії | 216,43±29,93 | 89,53±29,74 | 659,93±151,40 | 965,90±201,24 |
| Через 6 міс | 138,53±27,24* | 63,70±25,14 | 474,93±133,91 | 676,87±178,86** |
| Через 12 міс | 176,00±29,17* | 74,57±26,86 | 549,27±138,49 | 801,47±183,90** |
| 2-га група (ХС + диклофенак) | ||||
| До терапії | 213,10±32,96 | 89,30±25,07 | 603,30±150,59 | 905,70±191,91 |
| Через 6 міс | 151,53±27,38 | 64,60±21,60 | 451,03±132,37 | 665,83±171,23 |
| Через 12 міс | 184,63±29,17 | 77,50±24,60 | 537,83±148,25 | 800,07±193,90 |
| 3-тя група (німесулід) | ||||
| До терапії | 218,63±25,93 | 92,83±25,47 | 667,70±141,82 | 979,17±191,03 |
| Через 6 міс | 179,57±24,06 | 77,87±22,27 | 560,93±131,22 | 818,37±170,38 |
| Через 12 міс | 208,70±28,07 | 88,80±26,73 | 646,43±156,18 | 213,10±32,96 |
| 4-та група (диклофенак) | ||||
| До терапії | 212,90±33,60 | 83,20±26,00 | 629,17±134,94 | 925,27±182,39 |
| Через 6 міс | 176,33±30,44 | 69,33±22,32 | 539,13±125,15 | 784,80±168,27 |
| Через 12 міс | 208,77±36,93 | 82,23±32,24 | 626,53±148,63 | 917,20±207,10 |
*р<0,0001; **p<0,05.
Сумарний індекс WOMAC через 6 міс достовірно (р=0,006) знизився у 2-й групі (666,83±171,23 мм) порівняно з 3-ю групою (818,37±170,38 мм) (табл. 6). Також через 6 міс сумарний індекс WOMAC знизився у 1-й групі (676,87±178,86 мм) порівняно з 3-ю групою (р=0,016). Така ж тенденція збереглася і через 12 міс: сумарний індекс WOMAC у 2-й групі (800,07±193,90 мм) був достовірно нижчим (р=0,036), ніж у 3-й групі (944,93±201,51 мм).
Індекс Лекена через 6 міс у 1-й групі (11,27±2,35 бала) був достовірно нижчим (р=0,006) порівняно з 3-ю (13,33±2,26 бала) і нижчим (р=0,042) порівняно з 4-ю групою (12,9±2,2 бала). Індекс Лекена через 6 міс був нижчим і у 2-й групі (11,37±2,17 бала) порівняно з 3-ю та 4-ю групами (р<0,01).
Така динаміка альгофункціональних індексів WOMAC і Лекена свідчить про виражений анальгезивний і протизапальний ефект ХС-4,6.
Стандартні лабораторні показники не мали значимої динаміки в досліджуваних групах і перебували у межах вікової норми. Достовірну різницю спостерігали лише між рівнями СРП протягом спостереження. Через 6 міс від початку лікування рівень СРП у 1-й групі (4,21±1,33 мг/л) був достовірно нижчим (p=0,017), ніж у 3-й (5,50±1,84 мг/л), а також достовірно нижчим у 2-й групі (4,17±1,11 мг/л), ніж у 3-й (p=0,007) і 4-й (p=0,024). Через 1 рік від початку дослідження рівень СРП достовірно (p=0,047) був нижчим у 1-й групі (4,97±1,25 мг/л) порівняно з 3-ю (6,15±1,99 мг/л). Це свідчить про виражений протизапальний ефект ХС-4,6 і його стійкий ефект післядії.
| Група | Кількість загострень у пацієнтів | ||
|---|---|---|---|
| у середньому | із нормальною МЩКТ | зі зниженою МЩКТ | |
| 1-ша | 3,84±0,79* | 2,73±0,74 | 4,48±0,74 |
| 2-га | 3,91±0,52* | 2,38±0,55 | 4,98±0,63 |
| 3-тя | 6,84±0,72 | 5,54±0,46 | 7,54±0,72 |
| 4-та | 7,12±0,65 | 6,32±0,65 | 7,74±0,55 |
У табл. 7–9: *р<0,001.
Кількість загострень захворювання у групах хворих наведена в табл. 7. Відзначено достовірну різницю цього показника (р<0,01) у пацієнтів із нормальною МЩКТ та зі зниженою МЩКТ. Також достовірно (р<0,001) цей показник у 1-й групі був нижчим, ніж у 3-й групі (6,84±0,72), а також нижчим, ніж у 4-й групі (7,12±0,65) (р<0,001). Достовірно (р<0,001) цей показник у 2-й групі був також нижчим, ніж у 3-й групі (6,84±0,72), і нижчим, ніж у 4-й групі (7,12±0,65) (р<0,001). Середня тривалість застосування НПЗП та середня тривалість ефекту лікування після закінчення прийому НПЗП представлені в табл. 8 та 9 відповідно.
| Група | Тривалість прийому НПЗП у пацієнтів, днів | ||
|---|---|---|---|
| у середньому | з нормальною МЩКТ | зі зниженою МЩКТ | |
| 1-ша | 53,76±3,39* | 51,53±3,34 | 55,36±3,43 |
| 2-га | 54,74±4,38* | 53,38±1,06 | 56,04±4,21 |
| 3-тя | 95,76±5,32 | 92,04±5,66 | 96,74±5,51 |
| 4-та | 97,68±6,05 | 96,32±5,85 | 99,72±6,02 |
| Група | Тривалість ефекту у пацієнтів, тиж | ||
|---|---|---|---|
| у середньому | із нормальною МЩКТ | зі зниженою МЩКТ | |
| 1-ша | 12,44±1,09* | 13,73±1,24 | 11,58±1,43 |
| 2-га | 12,63±1,11* | 13,38±1,06 | 11,86±1,21 |
| 3-тя | 6,84±0,72 | 7,04±0,66 | 5,94±0,53 |
| 4-та | 5,95±0,65 | 6,32±0,65 | 5,02±0,55 |
Через півроку від початку дослідження при ультразвуковій денситометрії виявлено негативну динаміку показників МЩКТ (Т-і Z-індекси у SD) у 3-й і 4-й групах, де застосовували німесулід і диклофенак відповідно (рис. 2). Зниження Т-критерію в динаміці за 6 міс було достовірно (p<0,01) більш виражене у 4-й групі (–0,05±0,07 SD) порівняно з 1-ю (0,00±0,04 SD) та з 2-ю групою (0,00±0,03 SD). Негативну динаміку Z-індексу через 6 міс також відзначено у 3-й і 4-й групах. При цьому зниження Z-індексу в стандартних відхиленнях в динаміці за 6 міс достовірно (p=0,018) було більш виражене у 4-й групі (–0,04±0,06 SD) порівняно з 3-ю (–0,01±0,02 SD). Зниження Z-критерію в динаміці за 6 міс було достовірним (p=0,007) у 4-й групі (–0,04±0,06 SD) порівняно з 1-ю (0,00±0,04 SD). Це свідчить про те, що втрати кісткової маси у групах пацієнтів, які застосовували ХС-4,6, за 6 міс дослідження майже не спостерігалося, тоді як у групах, де використовували лише НПЗП, мало місце зниження МЩКТ, більш виражене у групі, де застосовували диклофенак.
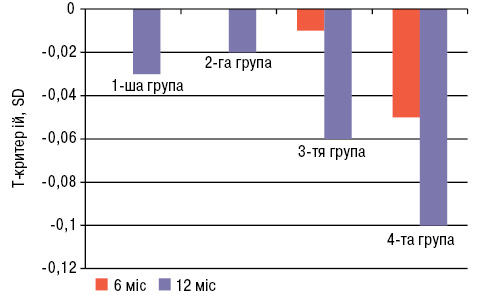
Рис. 2. Динаміка Т-критерію, SD
| Період | Група | |||
|---|---|---|---|---|
| 1-ша (ХС-4,6 + німесулід) | 2-га (ХС-4,6 + диклофенак) | 3-тя (німесулід) | 4-та (диклофенак) | |
| Т-індекс, SD | ||||
| 0–6 міс | 0,00±0,04(р=0,003 порівняно з 4-ю групою) | 0,00±0,03(р=0,007 порівняно з 4-ю групою) | –0,01±0,03 | –0,05±0,07 |
| 0–12 міс | –0,03±0,06(р=0,002 порівняно з 4-ю групою) | –0,02±0,05(р=0,0002 порівняно з 4-ю групою) | –0,06±0,07 | –0,10±0,08 |
| Z-індекс, SD | ||||
| 0–6 міс | 0,00±0,04(р=0,007 порівняно з 4-ю групою) | 0,00±0,03(р=0,007 порівняно з 4-ю групою) | –0,01±0,02(р=0,018 порівняно з 4-ю групою) | –0,04±0,06 |
| 0–12 міс | –0,02±0,06(р=0,002 порівняно з 4-ю групою) | –0,02±0,06(р=0,001 порівняно з 4-ю групою) | –0,05±0,07 | –0,09±0,07 |
Через рік від початку спостереження негативну динаміку показників МЩКТ відзначали вже у всіх групах пацієнтів (табл. 10). Зниження Т-критерію в динаміці за 12 міс було достовірно (p=0,0002) більш виражене у 4-й групі (–0,10±0,08 SD) порівняно з 2-ю групою (–0,02±0,05 SD). Зниження Т-критерію в динаміці за 12 міс також було достовірно (p=0,002) виражене у 4-й групі (–0,10±0,08 SD) порівняно з 1-ю групою (–0,03±0,06 SD). Негативна динаміка Z-індексу за 12 міс також була відзначена в усіх групах. При цьому зниження Z-індексу у стандартних відхиленнях в динаміці за 12 міс достовірно (p=0,003) було більш вираженим у 4-й групі (–0,09±0,07 SD) порівняно з 1-ю (–0,02±0,06 SD). Також зниження Z-індексу у стандартних відхиленнях в динаміці за 12 міс достовірно (p=0,001) було більш виражене у 4-й групі (–0,09±0,07 SD) порівняно з 2-ю групою (–0,02±0,06 SD). Динаміка показників МЩКТ за 12 міс спостереження свідчить про зниження МЩКТ в усіх групах спостереження, але в групах, де застосовували ХС-4,6, це зниження було менш вираженим. Така динаміка показників ультразвукової денситометрії свідчить про наявність позитивного впливу ХС-4,6 пташиного походження на метаболізм кісткової тканини.
Висновки
1. У хворих з остеодефіцитом встановлено більш виражений больовий синдром в колінному суглобі за ВАШ у спокої у середньому на 19,8% і при ходьбі — на 26,7%, за індексом WOMAC — на 19,6%, більш виражений показник обмеженості рухливості суглоба вранці та протягом дня за WOMAC у середньому — на 48%, показник обмеження повсякденної активності за WOMAC — на 27,8%, сумарний індекс WOMAC — на 27,2%, індекс Лекена — на 22,4%.
2. Спостерігалася достовірна різниця між рівнем ефективності ХС у хворих із нормальною та зниженою МЩКТ. 50% зниження показника WOMAC у хворих із нормальною МЩКТ досягнуто у 24% випадків, зі зниженою МЩКТ — лише в 11%.
3. У хворих на гонартроз зі зниженою МЩКТ спостерігали на 33% вищий рівень СРП на фоні більш тяжкого перебігу. У хворих на гонартроз відзначали незначний зворотний кореляційний зв’язок показників МЩКТ та рентгенологічної стадії гонартрозу (r=–0,314) і помірний зворотний кореляційний зв’язок показників МЩКТ та рівня СРП (r=–0,402).
4. Монотерапія диклофенаком має симптом-модифікуючу дію, зменшує вираженість клінічних проявів захворювання лише за фактом його застосування, що підтверджено динамікою альгофункціональних індексів WOMAC і Лекена, але не має клінічного ефекту післядії та не впливає на динаміку маркерів запалення.
6. При монотерапії гонартрозу із застосуванням німесуліду через 6 міс спостерігали достовірно меншу негативну динаміку показників МЩКТ (а саме Z-індексу у стандартних відхиленнях), ніж при монотерапії диклофенаком, що свідчить про позитивний вплив німесуліду на МЩКТ. Монотерапія німесулідом має симптом-модифікуючу дію, зменшує клінічні прояви захворювання лише за фактом його застосування, що підтверджено динамікою альгофункціональних індексів WOMAC і Лекена, але не має клінічного ефекту післядії та не впливає на динаміку маркерів запалення.
6. У всіх хворих на гонартроз ХС-4,6 виявив клінічну ефективність. У осіб з нормальною МЩКТ на фоні терапії ХС-4,6 виявлено більш значуще зниження рівня болю у колінних суглобах, зменшення скутості та обмеження у виконанні щоденної діяльності за анкетою WOMAС (р<0,05), а також рівня СРП (р<0,001) порівняно із хворими зі зниженою МЩКТ.
7. Виявлено позитивний вплив ХС-4,6 на динаміку показників МЩКТ. Протягом дослідження, через 6 і 12 міс встановлено достовірно менше зниження Т- і Z-індексів у стандартних відхиленнях за даними ультразвукової денситометрії у групах, де пацієнти приймали ХС-4,6, що свідчить про можливість ХС уповільнювати зниження МЩКТ у хворих на гонартроз.
8. Виявлений симптоматичний ефект та достовірний вплив на МЩКТ ХС є основою для застосування його як ефективного препарату у хворих зі зниженою МЩКТ.
СПИСОК ВИКОРИСТАНОЇ ЛІТЕРАТУРИ
- Arendt-Nielsen L., Hoeck H.C. (2011) Peripheral and Central Sensitisation in Osteoarthritis — Implication for Treatment. Eur. Musculoskel. Rev., 6(3): 158–161.
- Funck-Brentano T., Lin H., Hay E. et al. (2012) Targeting Bone Alleviates Osteoarthritis in Osteopenic Mice and Modulates Cartilage Catabolism. PLos One, 7(3): e33543.
- Iovu M., Dumais G., Souich P. (2008) Anti-inflammatory activity of chondroitin sulfate. Osteoarthritis Cartilage, 16: S14–8.4.
- Report of a WHO Study Group (1994) Assessment of fracture risk and its application to screening for postmenopausal osteoporosis. World Health Organ. Tech. Rep. Ser., 843: 1–129.
- Richette P., Funk-Brentano T. (2010) What is New on Osteoarthritis Front? Eur. Musculoskel. Rev., 5(2): 8–10.
- Souich P. (2009) Immunomodulatory and anti-inflammatory effects of chondroitin sulphate. Eur. Musculoske. Rev., 4(2): 8–10.
- Tat S.K., Pelletier J.P., Lajeunesse D. et al. (2008) The differential expression of osteoprotegerin (OPG) and receptor activator of nuclear factor kappaB ligand (RANKL) in human osteoarthritic subchondral bone osteoblasts is an indicator of the metabolic state of these disease cells. Clin. Exp. Rheumatol., 26: 295–304.
ДИФФЕРЕНЦИРОВАННЫЙ ПОДХОД В ЛЕЧЕНИИ при ГОНАРТРОЗе ПРОТИВОВОСПАЛИТЕЛЬНЫМИ ПРЕПАРАТАМИ В ЗАВИСИМОСТИ ОТ МИНЕРАЛЬНОЙ ПЛОТНОСТИ КОСТНОЙ ТКАНИ
Резюме. С целью определения дифференцированного подхода в лечении при гонартрозе противовоспалительными препаратами в зависимости от минеральной плотности костной ткани (МПКТ) оценены результаты исследования с участием 140 больных (128 женщин, 12 мужчин) гонартрозом II–III рентгенологической стадии по Kellgren — Lawrence. Всех больных гонартрозом, в зависимости от проводимой терапии, распределили на четыре равные группы по 35 пациентов. Пациенты 1-й группы принимали хондроитин сульфат (ХС)-4,6 птичьего происхождения по 500 мг 2 раза в сутки в течение 6 мес и нимесулид в гранулированной форме 100 мг 2 раза в сутки до 15 дней. Пациенты 2-й группы принимали ХС-4,6 по 1 г/сут в течение 6 мес и диклофенак 50 мг 3 раза в сутки до 15 дней. Пациенты 3-й группы принимали только нимесулид 200 мг/сут до 15 дней. Пациенты 4-й группы принимали диклофенак 150 мг/сут до 15 дней. При выраженном болевом синдроме курс терапии нестероидными противовоспалительными препаратами повторяли с интервалом не менее 2 нед. Через полгода после начала исследования при ультразвуковой денситометрии выявлена отрицательная динамика Т- и Z-индекса за 6 мес в стандартных отклонениях в 3-й и 4-й группах больных, но через 1 год отрицательная динамика отмечалась уже у больных всокех групп, причем достоверно меньше у пациентов 1-й и 2-й групп, которые применяли ХС. Через 6 мес выявлено достоверное снижение Z-индекса у больных 4-й группы по сравнению с 3-й группой, что свидетельствует о том, что потери костной массы у больных 3-й группы были достоверно менее значимые. Таким образом, выявлено положительное влияние ХС на МПКТ. Отмечена высокая клиническая эффективность и выраженный эффект последействия ХС у пациентов с гонартрозом II–III рентгенологической стадии по Kellgren — Lawrence.
остеоартроз коленных суставов, WOMAC, минеральная плотность костной ткани, хондроитин сульфат, нимесулид, диклофенак.
Адреса для листування:
Шуба Неоніла Михайлівна
04112, Київ, вул. Дорогожицька, 9
Національна медична академія післядипломної
освіти ім. П.Л. Шупика

Leave a comment