Ризик розвитку та особливості нефропатії у хворих на системну склеродермію
Курята О.B.1, Лисунець Т.К.2, Караванська І.Л., Семенов В.В.1
- 1ГУ «Днепропетровская медицинская академия МЗ Украины»
- 2КЗ «Обласна клінічна лікарня ім. І.І. Мечникова», Дніпропетровськ
Резюме. Досліджували ризик розвитку та особливості перебігу нефропатії у хворих на системну склеродермію (ССД). У 5-річному проспективному спостереженні взяв участь 81 пацієнт з ССД . Учасники знаходяться у регіональному реєстрі, проходять регулярні обстеження та отримують медичну допомогу у ревматологічному стаціонарі. Встановлено, що у пацієнтів із дифузною ССД більш виражені фібротичні зміни — пневмофіброз та ущільнення шкіри, а у осіб із лімітованою ССД частіше визначали ознаки судинної патології — артеріальної гіпертензії (АГ). Найбільш раннім та надійним маркером ураження нирок є протеїнурія. Частота АГ корелює зі ступенем нефропатії.
Вступ
Системна склеродермія (ССД) на сьогодні — одне з найменш досліджених ревматологічних захворювань, незважаючи на значну еволюцію в уявленнях про природу хвороби. Найвища летальність при ССД пов’язана з легеневими ускладненнями (Solomon J.J. et al., 2013), проте прогноз захворювання часто визначається ураженням нирок, яке відзначають у більше ніж 10–20% хворих (Varga J. et al., 2012). Результати досліджень свідчать про значний зв’язок між ураженням нирок та прогнозом хвороби, зокрема утричі вищу смертність від легеневої гіпертензії за наявності ниркової недостатності (Shanmugamand V.K., Steen V.D., 2010).
ССД — тяжке мультисистемне захворювання, в основі якого — ураження ендотелію з порушенням мікроциркуляції та дифузні склеротичні зміни сполучної тканини. Згідно зі світовою статистикою, середня захворюваність у світі коливається від 0,6 до 19 на 1 млн населення, поширеність — 4–242 на 1 млн населення (Hunzelmann N. et al., 2008). Захворювання у 3–8 разів частіше діагностують у жінок, дебют захворювання припадає на вік від 45 до 54 років (Silman A.J., 1991). Офіційної статистики щодо ССД в Україні немає, але відомо, що захворюваність та поширеність хвороб кістково-м’язової системи та сполучної тканини, за даними на 2013 р., становила 3182,3 та 9977,0 на 100 тис. населення, смертність від цих хвороб — 1,3 на 100 тис. населення (Коваленко В.М., Корнацький В.М., 2014).
Незважаючи на інтенсивне вивчення питань етіології та патогенезу ССД протягом останніх десятиліть, багато що залишається невідомим. У 70-ті роки XX ст. спостерігався стрибок захворюваності без подальшої тенденції до підвищення (Mayes M.D., 2003; Varga J. et al., 2012). На основі цих даних неодноразово намагалися пов’язати виникнення захворювання з екзогенними факторами, у ряді випадків такий зв’язок було виявлено. Найцікавіші дослідження стосуються впливу кремнієвих сполук, зокрема виявлена вища захворюваність на ССД в японських жінок, яким була проведена пластика грудей силіконовими або парафіновими імплантатами. Генетичні фактори мають певне значення у розвитку захворювання, але їх значення до кінця не вивчене. Вплив шкідливих звичок на ризик розвитку ССД не вивчений, але є дані, що ССД частіше розвивається у людей, які часто контактують із тваринами (Silman A.J., 1991).
Патогенез ССД — складний та, вірогідно, пов’язаний з ендотеліальними, епітеліальними клітинами, фібробластами та імунологічними посередниками. У результаті порушується регуляція судинного ремоделювання та, врешті-решт, розвивається васкулопатія. Пошкодження ендотелію є ранньою та, ймовірно, первинною подією, але точний пусковий фактор залишається невідомим. Виявлена схожість у перебігу васкулопатії в різних органах, та вважається, що важливу роль у цьому процесі відіграє ендотелін (ЕТ)-1. У пацієнтів із ССД спостерігається надекспресія ET-1, його концентрація в сироватці крові корелює з тяжкістю захворювання (Mayes M.D., 2003). Існує думка, що первинною ланкою патогенезу ССД є активація Т-лімфоцитів у результаті дії факторів навколишнього середовища та спадковості. Дія Т-лімфоцитів призводить до ураження ендотелію та активації фібробластів (Гусева Н.Г., 2002).
Клінічні прояви ураження нирок варіюють від гострої склеродермічної нирки до субклінічної нефропатії. Гостру нефропатію діагностують у 5–10% хворих на ССД (Simeón-Aznar C.P. et al., 2012). Порушення функції нирок або протеїнурію виявляють у ≈⅓ хворих на ССД (Steen V.D. et al., 2005). Смертність від ниркових ускладнень знизилася з 76 до 15% у США завдяки рутинному застосуванню інгібіторів ангіотензинперетворювального ферменту (іАПФ) (Steen V.D. et al., 1990). Незважаючи на це, летальність від ниркових ускладнень залишається високою: 15-тирічна виживаність без ураження нирок становить 73%, при ураженні нирок — 13%. 5-Річна виживаність у пацієнтів із нефропатією становить 23% (Гусева Н.Г., 2002). Хронічна хвороба нирок (ХХН), що розвинулася на тлі ССД, у 0,3% випадків потребує проведення пожиттєвого діалізу (Siva B. et al., 2011).
Лікування пацієнтів із хронічною нирковою недостатністю (ХНН) термінальної стадії досить високовартісне та водночас малоефективне, тому є сенс шукати симптоми, що асоціюються з агресивним перебігом хвороби. Близько 50% пацієнтів із безсимптомним перебігом нефропатії мають такі ознаки, як підвищення рівня креатиніну, протеїнурію чи артеріальну гіпертензію (АГ). Альбумінурія —зручний маркер ангіопатії — вважається незалежним предиктором кардіоваскулярних ускладнень і смертності. Протеїнурія корелює з давністю хвороби >4 років та АГ. Наявність протеїнурії вважають відображенням ураження судин (Shanmugamand V.K., Steen V.D., 2010). У наукових роботах, присвячених ураженням внутрішніх органів, зокрема нирок, при
ССД, протеїнурія та АГ розглядаються ізольовано, без урахування комбінації цих ознак (Walker U.A. et al., 2007; Hunzelmann N. et al., 2008; Shanmugamand V.K., Steen V.D., 2010; Simeón-Aznar C.P., et al., 2012).
Мета дослідження — проаналізувати ризик розвитку та особливості перебігу нефропатії у хворих на CCД.
ОБ’ЄКТ І МЕТОДИ ДОСЛІДЖЕННЯ
Дизайн дослідження
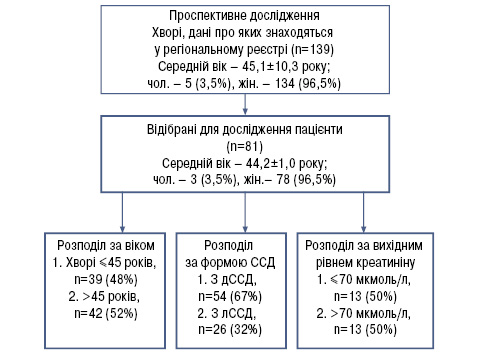
Засновано регіональний реєстр хворих на ССД, який містить дані про 139 пацієнтів із ССД віком від 17 до 71 року (5 чоловіків та 134 жінки), середній вік M±m — 45,1±1,0 року, які спостерігаються з 1993 р. Максимальний термін спостереження — 21 рік. Проведене 5-річне проспективне спостереження хворих на ССД, які проходять регулярні обстеження й отримують медичну допомогу в ревматологічному стаціонарі. Досліджено дані 81 пацієнта із ССД віком від 20 до 71 року (3 (3,5%) чоловіків та 78 (96,5%) жінок), середній вік M±m — 44,2±1,0 року. Один пацієнт помер (склеродермічний нирковий криз), в одного розвинувся хронічний лімфолейкоз. Чисельна перевага жінок у дослідженні зумовлена більшою розповсюдженістю захворювання серед осіб жіночої статі (Silman A.J., 1991).
Критерії включення:
- верифікований діагноз ССД (Наказ МОЗ України від 12.10.2006 р. № 676);
- інформована згода пацієнта на збір та обробку даних.
Критерії виключення:
- гостре ураження нирок;
- протеїнурія >3,5 г/добу;
- гострий коронарний синдром;
- хронічна серцева недостатність IV функціонального класу (NYHA);
- АГ II та III ступеня, що не контролювалася медикаментозно;
- некомпенсований цукровий діабет;
- індекс маси тіла (ІМТ) <18,5 кг/м;
- термінальна стадія ХНН (швидкість клубочкової фільтрації (ШКФ) <30 мл/хв).
З урахуванням критеріїв включення та виключення з дослідження, була сформована вибірка з пацієнтів, які проходили регулярні обстеження в ревматологічному відділенні — 81 пацієнт (3 чоловіки та 78 жінок) віком від 20 до 71 року, середній вік — M±m 44,2±1,0 року.
У подальшому проведено субаналіз клінічних проявів нефропатії у пацієнтів із ССД залежно від віку, форми захворювання чи вихідного рівня креатиніну в сироватці крові.
Розподіл вихідного рівня креатиніну в сироватці крові у пацієнтів наближався до бімодального з перехідним значенням 70 мкмоль/л. Тому пацієнтів розподілили на дві групи — з креатиніном у сироватці крові >70 та ≤70 мкмоль/л (рис. 1).
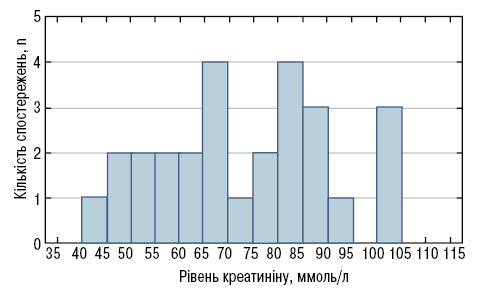
Рис. 1. Вихідний рівень креатиніну сироватки крові в учасників дослідження (n=26)
Методи дослідження і статистичної обробки даних
Усім (n=81) хворим проводили клінічне обстеження, інструментальне та лабораторне дослідження згідно із загальноприйнятими стандартними критеріями (Наказ МОЗ України від 12.10.2006 р. № 676) (рис. 2).
Наявність АГ верифіковано за допомогою класифікації, прийнятої в Україні й рекомендованої для застосування у практиці (Наказ МОЗ України від 14.02.2002 р. № 54). АГ визначали при стабільному підвищенні артеріального тиску (АТ) >140/90 мм рт. ст. АТ вивчали методом аускультації тонів М.С. Короткова з використанням тонометра. На плече пацієнта (на 2–3 см вище ліктьової ямки) накладали манжетку тонометра, прикладали фонендоскоп у ліктьовому згині у проекції плечової артерії. Повітря нагнітали в манжетку на 30 мм рт. ст. вище рівня, при якому зникала пульсація плечової артерії. Систолічний АТ реєстрували з моменту першої появи тонів, діастолічний — після повного зникнення тонів. АТ вимірювали тричі після 5-хвилинного відпочинку.
Усім хворим проводили загальний аналіз крові та сечі. Ревматоїдний фактор (РФ) визначали за допомогою реакції Ваалера — Роуза, кріоглобуліни — напівкількісним методом, С-реактивний білок (СРБ) — турбідиметричним методом. Досліджували загальні циркулюючі імунні комплекси (ЦІК) методом селективної преципітації з 3,5% розчином поліетиленгліколю-6000 з подальшим визначенням оптичної щільності досліджуваного розчину (Haskova V., 1978).
Для клінічної оцінки функції нирок визначали рівень креатиніну в сироватці крові за допомогою колориметричних методів та наявність протеїнурії турбідиметричним методом і обчислювали ШКФ за формулою GFR (glomerular filtration rate)-ЕРІ (Andrew S. et al., 2009):
Для чоловіків:
ШКФ = 141 ⋅ min (сКр/0,9, 1)×
× max (сКр/0,9, 1) 0,993
Для жінок:
ШКФ = 141 ⋅ min (сКр/0,7, 1)×
× max (сКр/0,7, 1) 0,993 1,018,
де: сКр — креатинін у сироватці крові, min — мінімальний, max — максимальний рівень креатиніну.
Протеїнурію діагностували при екскреції білка з сечею >0,3 та <3,5 г/добу (Наказ МОЗ України від 02.12.2004 р. № 593). Для виключення сечокам’яної хвороби проводили ультразвукове дослідження нирок. Слід зауважити, що нами не проводилося дослідження морфології нирок. Саме тому ми уникаємо вживання терміну «нефропатія», так само, як і європейські дослідники (Walker U.A. et al., 2007; Hunzelmann N. et al., 2008; Simeón-Aznar C.P. et al., 2012).
Усім хворим проводили електрокардіографічне дослідження (ЕКГ) за допомогою електрокардіографа ЕКЗТ-01-«РЯ». ЕКГ реєстрували у 12 відведеннях: у 6 від кінцівок (І, ІІ, ІІІ, aVR, aVL, aVF), і у 6 — грудних (V1–V6) з реєстрацією не менше 4 передсердно-шлуночкових комплексів.
За даними рентгенологічного дослідження легень виявляли ознаки пневмофіброзу.
Лікування зазначених хворих проводили згідно з наказом МОЗ України від 12.10.2006 р. № 676 «Клінічний протокол надання медичної допомоги хворим із системною склеродермією».
Дані обробляли методом варіаційної статистики для малих вибірок за допомогою програмного забезпечення Microsoft Excel та STATISTICA 10.0 (Реброва О.Ю., 2002). Цей метод включав обчислення середнього арифметичного (М), середнього квадратичної похибки від середнього арифметичного. При порівнянні частот ураження внутрішніх органів використовували t-критерій Стьюдента для порівняння відносних величин. При порівнянні залежних вибірок використовували t-критерій Вілкоксона. Критичне значення р при перевірці статистичних гіпотез приймалося рівним 0,05.
РЕЗУЛЬТАТИ ТА ЇХ ОБГОВОРЕННЯ
Клінічна характеристика хворих на ССД
Основні загально-клінічні характеристики пацієнтів наведені у табл. 1–4.
За даними дослідження початок захворювання припадав на вік 44,2±1,0 року. У структурі хворих переважали жінки (див. табл. 1), що зіставне з даними німецького та іспанського реєстрів, але за даними реєстру EULAR середній вік початку хвороби був дещо старшим (Walker U.A. et al., 2007; Hunzelmann N. et al., 2008; Simeón-Aznar C.P. et al., 2012). У представленому дослідженні переважають пацієнти із дССД. Така кардинальна відмінність від загальної тенденції може бути пояснена пізнім зверненням пацієнтів.
| Показник | Кількість хворих, n (%) | Середній вік, років (M±m) | |
|---|---|---|---|
| Стать | Чоловіки | 3 (3,5) | 38,6±9,5 |
| Жінки | 78 (96,5) | 44,4±1 | |
| Форма ССД | Лімітована | 26 (32) | 44,3±1,9 |
| Дифузна | 54 (67) | 44±1,2 | |
| Вік, років | ≤45 років | 39 (48) | 37,1±1,1 |
| >45 років | 42 (52) | 51,0±0,7 | |
| Показник | Кількість хворих, n (%) | |
|---|---|---|
| Клінічні ознаки | Набряк кистей | 47 (57) |
| Артрит | 71 (86) | |
| Пневмофіброз | 19 (23) | |
| АГ | 19 (23) | |
| Лабораторні ознаки | Анемія | 11 (13) |
| Протеїнурія | 22 (27) | |
| СРБ >6 мг/л | 29/72 (40) | |
| РФ >12 мОд/мл | 8/56 (14) | |
| ЦІК >0,05 | 49/57 (86) | |
| Кріоглобулінемія | 30/54 (55) | |
Найпоширенішими симптомами на початку хвороби є артрит (86%) та щільний набряк кистей (57%) (див. табл. 1). Рівень ЦІК асоціюється з клінічним перебігом захворювання (Курята О.В. и соавт., 2006).
Клінічні та лабораторні симптоми відрізнялися у пацієнтів різних вікових груп та з різними формами захворювання, причому різниця була найбільш вираженою між пацієнтами з дССД та лССД (див. табл. 3, 4).
Так, в обох групах (дССД та лССД) приблизно з однаковою частотою виявляли ознаки імунокомплексного запалення — артрит і підвищення ЦІК, але у пацієнтів із дССД більш вираженими були фібротичні зміни — пневмофіброз при ураженні шкіри, а у пацієнтів із лССД частіше визначали ознаки судинної патології — АГ (див. табл. 3).
| Показник | Кількість хворих, n (%) | ||
|---|---|---|---|
| лССД (n=26) | дССД (n=54) | ||
| Клінічні ознаки | Набряк кистей | 9 (35) | 38 (70)* |
| Артрит | 23 (88) | 47 (87) | |
| Пневмофіброз | 1 (4) | 17 (31)* | |
| АГ | 8 (31) | 11 (20) | |
| Лабораторні ознаки | Анемія | 2 (8) | 9 (17) |
| Протеїнурія | 5 (19) | 17 (31) | |
| СРБ >6 мг/л | 8/25 (32) | 20/46 (43) | |
| РФ >12 мОд/мл | 1/19 (5) | 7/36 (19) | |
| ЦІК >0,05 | 17/20 (85) | 31/36 (86) | |
| Кріоглобулінемія | 8/19 (42) | 21/34 (62)* | |
У табл. 3 і 4: *p<0,05.
Згідно з даними літератури, переважання фібротичних змін у тканинах над іншими (судинні, запальні) частіше відзначають при гострому та швидко прогресуючому перебігу хвороби (Гусева Н.Г., 2007). Генералізований фіброз частіше поєднується зі склеродермічною нефропатією та асоціюється з несприятливим прогнозом (5-річна виживаність — 4%) (Гусева Н.Г., 2007).
При порівнянні груп хворих на ССД за віком помітна дещо вища активність процесу та переважання пацієнтів з АГ у старшій групі, що може бути наслідком вікового ураження судин (див. табл. 4).
| Показник | Кількість хворих, n (%) | ||
|---|---|---|---|
| Вік ≤45 років (n=39) | Вік >45 років (n=42) | ||
| Клінічні ознаки | Набряк кистей | 22 (56) | 25 (60) |
| Артрит | 33 (85) | 38 (90) | |
| Пневмофіброз | 4 (10) | 15 (36)* | |
| АГ | 3 (8) | 16 (38)* | |
| Лабораторні ознаки | Анемія | 5 (13) | 6 (14) |
| Протеїнурія | 5 (12) | 12 (31) | |
| СРБ >6 мг/л | 10/35 (29) | 19/37 (51)* | |
| РФ >12 мОд/мл | 3/29 (10) | 5/27 (18) | |
| ЦІК >0,05 | 19/24 (79) | 30/33 (90) | |
| Кріоглобулінемія | 13/23 (56) | 17/31 (55) | |
В опублікованих раніше дослідженнях підіймалося питання про ураження нирок у хворих на ССД та виділення ознак, що асоціюються з нефропатією. Зокрема, в іспанському реєстрі дослідження ниркових ускладнень обмежується вивченням гострого склеродермічного нефриту, хоча наслідки ХХН, спричинені ССД, не менш тяжкі та потребують дорогого і тривалого лікування (Simeón-Aznar C.P., 2012). У реєстрі EUSTAR представлена поширеність не лише гострого ураження нирок при ССД, але й частота виникнення протеїнурії та АГ у хворих на лССД та дССД (Walker U.A. et al., 2007). Частота виявлення цих симптомів, згідно з даними EUSTAR, була значно нижчою, ніж у представленому дослідженні. Найповніше проблема нефропатії у хворих на ССД розкрита у дослідженні N. Hunzelmann та співавторів (2008), де представлена частота АГ, протеїнурії та ниркової недостатності (ШКФ <80 мл/хв). При порівнянні наших результатів з даними німецького реєстру (Hunzelmann N. et al., 2008), видно, що поширеність АГ серед хворих на ССД взагалі та у групах за формою хвороби майже не відрізняється. Проте рівень протеїнурії за нашими даними був значно вищим. Причина вищої частоти ознак ураження нирок у хворих на ССД у нашому дослідженні може полягати у пізній діагностиці лікарями первинної ланки та несвоєчасному зверненні до лікаря-ревматолога. Також до таких наслідків може призводити менша прихильність лікарів порівняно з європейськими колегами до застосування іАПФ, що зменшують протеїнурію. З іншого боку, відміни у перебігу хвороби витікають із різного етнічного складу населення у Східній та Західній Європі. У мультицентровому дослідженні, присвяченому гострому ураженню нирок при ССД (Guillevin L. et al., 2012) виявлено підвищений ризик щодо розвитку гострого склеродермічного нефриту у пацієнтів з АГ.
Нами розглянуто поширеність комбінації АГ та протеїнурії. Враховуючи вік початку захворювання (у нашому дослідженні він становив 44,2±1,0 року), а також вищу поширеність АГ серед пацієнтів старшої групи, можна припустити, що її розвиток пов’язаний не лише з нирковою патологією. АГ, що з’явилася на тлі ССД, може бути результатом ушкодження ниркових судин, але в такому разі було б більш коректно розглядати її разом із протеїнурією. Також виявлено, що у пацієнтів, які мають комбінацію АГ + протеїнурія, функція нирок порівняно з іншими пацієнтами суттєво знижена, тому такі пацієнти становлять групу підвищеного ризику розвитку термінальної стадії ХНН (табл. 5).
| Показник | Кількість хворих, n (%) | |
|---|---|---|
| Клінічні ознаки | Набряк кистей | 9 (82) |
| Артрит | 9 (82) | |
| Пневмофіброз | 4 (36) | |
| Лабораторні ознаки | Анемія | 0 (0) |
| СРБ >6 мг/л | 3 (27) | |
| РФ >12 мОд/мл | 1 (9) | |
| ЦІК >0,05 | 9/9 (100) | |
| Кріоглобулінемія | 4/9 (44) | |
| Креатинін, мкмоль/л | 82,6±6,6 | |
| ШКФ, мл/хв | 67,9±7,9 | |
Один пацієнт, в якого виявлено нефропатію, помер на другому році хвороби від склеродермічного ниркового кризу.
Клінічні прояви нефропатії у хворих на ССД залежно від віку
У пацієнтів молодого віку (≤45 років) комбінація АГ + протеїнурія на початку дослідження не визначалася, через 3 роки спостерігалася у 1 (2,5%), через 5 років — у 2 (5%) хворих. Протеїнурію на першому році дослідження виявлено — у 12 (31%) , через 3 роки — у 17 (43%), через 5 років — у 21 (54%) пацієнта. АГ у перший рік — у 3 (7%), через 3 роки — у 5 (13%), через 5 років — у 5 (13%) пацієнтів. Креатинін у сироватці крові на початку дослідження — 67,6±5,2 мкмоль/л, через 3 роки — 71,6±6,0 мкмоль/л, через 5 років — 71,6±4,1 мкмоль/л. ШКФ на початку дослідження — 108,0±13,8 мл/хв, через 3 роки — 95,9±8,8 мл/хв, через 5 років — 94,4±8,7 мл/хв.
У пацієнтів віком >45 років комбінацію АГ + протеїнурія на початку дослідження виявлено у 5 (12%), через 3 роки — у 7 (17%), через 5 років — у 9 (21%) пацієнтів. Протеїнурію на початку дослідження зареєстровано — у 9 (22%), через 3 роки — у 12 (29%), через 5 років — у 16 (39%) пацієнтів. АГ на початку дослідження — у 15 (36%), через 3 роки — у 19 (46%), через 5 років — у 21 (51%) пацієнта. Креатинін у сироватці крові на початку дослідження — 75,8±4,0 мкмоль/л, через 3 роки — 77,8±3,0 мкмоль/л, через 5 років — 70,0±2,7 мкмоль/л. ШКФ на початку дослідження — 81,4±7,36 мл/хв (p<0,05), через 3 роки — 75,7±5,5 мл/хв (p<0,05), через 5 років — 85,9±5,0 мл/хв.
Динаміку рівня креатиніну в сироватці крові у хворих на ССД залежно від віку протягом 5 років представлено на рис. 3.
На рис. 4 представлено динаміку ШКФ у хворих на ССД залежно від віку протягом 5 років.
Незважаючи на те що вихідна частота ураження нирок була вищою у пацієнтів старшого віку, її наростання було менш вираженим, ніж у молодших осіб. Такий висновок зроблено, ґрунтуючись на тому, що маркером ураження нирок у більшості випадків ставала протеїнурія, причому саме у молодших пацієнтів. Частота нефропатії, як і частота АГ, була суттєво вищою у пацієнтів старшого віку, але у них же зафіксована більша поширеність АГ на початку хвороби, що може бути пояснене еволюційними процесами. Рівень креатиніну в сироватці крові у пацієнтів старшого віку залишався стабільним. У молодших пацієнтів рівень креатиніну мав тенденцію до наростання зі збільшенням тривалості хвороби. Таке явище може бути пояснене більшою увагою до пацієнтів із початково ураженими нирками як з боку лікарів, так і з боку самих пацієнтів.
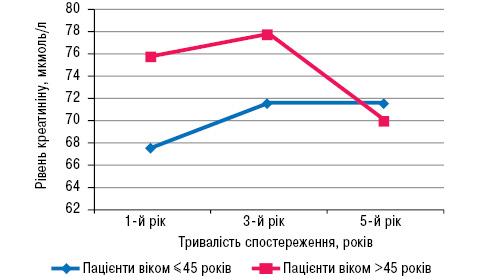
Рис. 3. Динаміка рівня креатиніну в сироватці крові у хворих на ССД залежно від віку протягом 5 років
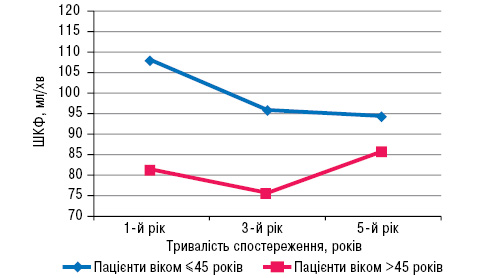
Рис. 4. Динаміка ШКФ у пацієнтів із ССД залежно від віку протягом 5 років
Клінічні прояви нефропатії у хворих на ССД залежно від форми захворювання
У пацієнтів із дССД на початку дослідження комбінацію АГ + протеїнурія визначали у 3 (6%), через 3 роки — у 4 (7%), через 5 років — у 6 (11%) пацієнтів. Протеїнурію у перший рік дослідження виявляли у 17 (31%), через 3 роки — у 23 (43%), через 5 років — у 29 (54%) пацієнтів. АГ на першому році спостерігалася у 11 (20%), через 3 роки — у 15 (28%), через 5 років — у 17 (31%) пацієнтів. Рівень креатиніну в сироватці крові на початку дослідження — 71±3,4 мкмоль/л, через 3 роки — 72,5±2,7 мкмоль/л, через 5 років — 69,0±2,8 мкмоль/л. ШКФ на початку дослідження — 94,4±8,0 мл/хв, через 3 роки — 89,8±6,4 мл/хв, через 5 років — 93,5±6,2 мл/хв.
У пацієнтів із лССД на початку дослідження комбінація АГ + протеїнурія спостерігалась у 3 (12%), через 3 роки — у 4 (15%), через 5 років — у 5 (19%) осіб. Протеїнурію у перший рік виявлено у 5 (19%), через 3 роки — у 7 (27%), через 5 років — у 8 (31%) пацієнтів. АГ на початку дослідження відзначали у 8 (31%), через 3 роки — у 10 (38%), через 5 років — у 10 (38%) пацієнтів. Рівень креатиніну в сироватці крові на початку дослідження — 80,7±3,8 мкмоль/л, через 3 роки — 79,0±4,0 мкмоль/л, через 5 років — 72,5±5,4 мкмоль/л. ШКФ на початку дослідження — 95,2±25,5 мл/хв, через 3 роки — 62,5±11,2 мл/хв, через 5 років — 83,3±9,6 мл/хв.
У пацієнтів із лімітованою формою ССД частіше відзначали комбінацію АГ + протеїнурія, тоді як у хворих із дифузною формою частіше ці ознаки виявлялися окремо. В обох групах маркером нефропатії частіше була протеїнурія. За даними реєстру EULAR, у пацієнтів із дССД слід очікувати високу частоту протеїнурії, що підтверджено нашим дослідженням. В обох групах хворих на ССД середній рівень креатиніну залишався стабільним. Слід зазначити, що у пацієнтів, які мали комбінацію АГ + протеїнурія, рівень креатиніну становив >70 мкмоль/л, а ШКФ <90 мл/хв, тому у осіб із лССД у проведеному дослідженні можна очікувати більш несприятливий прогноз щодо розвитку ХНН. Це не є типовим, оскільки опубліковані раніше дані свідчать, що при лССД перебіг ураження нирок відбувається м’якше. Виявлена закономірність потребує подальшого дослідження.
Клінічні прояви нефропатії у хворих на ССД залежно від вихідного рівня креатиніну в сироватці крові
У пацієнтів із початковим рівнем креатиніну ≤70 мкмоль/л (1-ша група) — комбінація АГ + протеїнурія не була зафіксована ні на початку дослідження, ні через 5 років. Протеїнурію на початку дослідження визначали у 3 (25%), через 3 роки — у 5 (42%), через 5 років — у 7 (58%) пацієнтів. АГ на першому році діагностували у 1 (8%), через 3 роки — у 1 (8%), через 5 років — у 1 (8%) пацієнта. Рівень креатиніну в сироватці крові на початку дослідження становив — 58,6±2,4 мкмоль/л, через 3 роки — 62,1±3,0 мкмоль/л, через 5 років — 59,2±2,1 мкмоль/л. ШКФ на початку дослідження — 121±9,6 мл/хв, через 3 роки — 109,3±8,7 мл/хв, через 5 років — 116,3±9,1 мл/хв.
У пацієнтів із початковим рівнем креатиніну >70 мкмоль/л (2-га група) — комбінацію АГ + протеїнурія на початку дослідження визначали у 2 (14%), через 3 роки — у 3 (21%), через 5 років — у 5 (35%) пацієнтів. Протеїнурію на початку відзначали у 5 (36%), через 3 роки — у 6 (43%), через 5 років — у 9 (64%) пацієнтів. АГ на першому році діагностували у 5 (36%), через 3 роки — у 7 (50%), через 5 років — у 9 (64%) пацієнтів. Рівень креатиніну в сироватці крові на початку дослідження — 86,0±2,6 мкмоль/л, через 3 роки — 78,1±4,1 мкмоль/л, через 5 років — 73,0±3,2 мкмоль/л. ШКФ на початку дослідження — 64,0±2,7 мл/хв, через 3 роки — 73,9±6,3 мл/хв, через 5 років — 80,6±4,2 мл/хв (р<0,05).
Серед пацієнтів із початково низьким креатиніном комбінацію АГ + протеїнурія не виявлено у жодного пацієнта. Серед учасників дослідження, які мали низький початковий креатинін, АГ діагностували значно рідше, ніж в іншій групі, що обмежує використання АГ як маркера ураження нирок у цих пацієнтів (рис. 5).
В обох групах маркером ураження нирок найчастіше була протеїнурія.
У пацієнтів 1-ї групи рівень креатиніну наростав зі збільшенням тривалості захворювання, на відміну від пацієнтів 2-ї групи.
При обчисленні ШКФ в обох групах було з’ясовано, що у 2-й групі пацієнтів ШКФ була суттєво нижчою, ніж у 1-й, хоча й дещо збільшувалася із тривалістю хвороби (р<0,05), тоді як у 1-й групі показник ШКФ за 5 років дещо знизився (рис. 6).
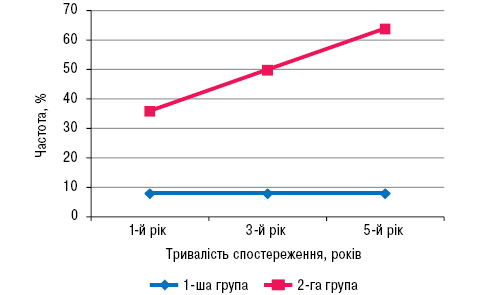
Рис. 5. Частота АГ залежно від вихідного рівня креатиніну протягом 5 років
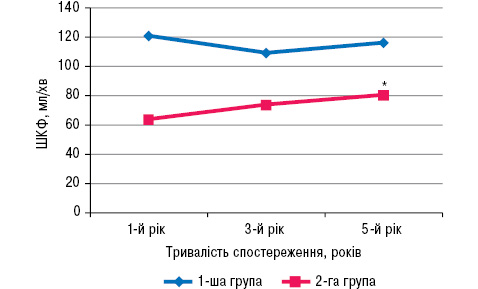
Рис. 6. Динаміка ШКФ залежно від його вихідного рівня протягом 5 років. На рис. 6 і 7: *р<0,05
Такі дані свідчать про те, що терапія, яка проводилася цим пацієнтам, ефективна. З вищесказаного також виходить, що усі пацієнти, незалежно від ступеня ураженості внутрішніх органів, потребують агресивної терапії.
Прогноз розвитку нефропатії у хворих на ССД протягом 5 років
На початку спостереження комбінацію АГ + протеїнурія виявлено у 5 (6%), через 3 роки — у 8 (10%), через 5 років — у 11 (13,5%) пацієнтів (рис. 7).
У перший рік протеїнурію виявлено у 22 (27%), через 3 роки — у 33 (41%), через 5 років — у 43 (53%) пацієнтів (див. рис. 7). АГ початково діагностували у 19 (23%) , через 3 роки — у 26 (32%), через 5 років — у 31 (38%) пацієнта (див. рис. 7). ШКФ на початку спостереження становила 92,7±7,5 мл/хв, через 3 роки — 85,7±5,4 мл/хв, через 5 років — 90,1±5,0 мл/хв.
Відомо, що креатинін не є надійним симптомом ураження нирок у хворих на ССД (Shanmugamand V.K., Steen V.D., 2010) Це підтверджують результати проведеного нами дослідження: рівень креатиніну в сироватці крові не зростав, а частота проявів ураження нирок, таких як поява протеїнурії та АГ, підвищувалася.
Середній рівень креатиніну в сироватці крові на початку дослідження становив 72,3±3,2 мкмоль/л, через 3 роки — 74,7±2,5 мкмоль/л, через 5 років — 70,0±2,4 мкмоль/л.
За результатами проведеного дослідження ризик розвитку АГ у хворих на ССД у 5-річній перспективі становить 15% (рис. 8).
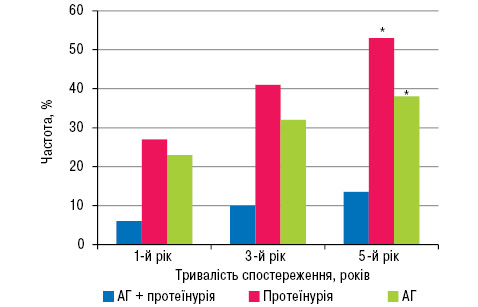
Рис. 7. Динаміка розвитку нефропатії у хворих на ССД.
Ризик розвитку протеїнурії за той самий період становить 25% (рис. 9).
Критичний термін розвитку обох симптомів — 3 роки.
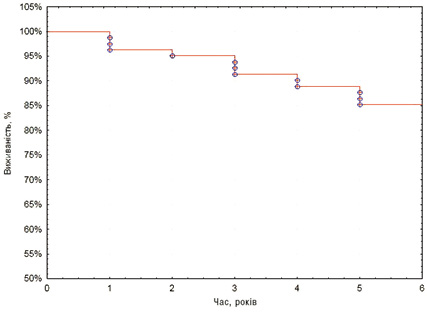
Рис. 8. Частка пацієнтів із ССД, які залишилися нормотензивними протягом 5 років
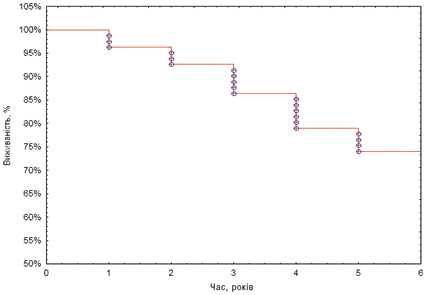
Рис. 9.Частка пацієнтів із ССД, в яких не розвинулася протеїнурія протягом 5 років
Висновки
1. Середній вік початку захворювання пацієнтів становив 44,2±1,0 року. У структурі хворих на ССД переважають жінки. Найбільш поширеними симптомами на початку хвороби є артрит (86%) та щільний набряк кистей (57%). У пацієнтів із дССД більш вираженими були фібротичні зміни — пневмофіброз при ураженні шкіри, а у пацієнтів із лССД частіше визначали ознаки судинної патології — АГ. Виявлено вищу поширеність пневмофіброзу та АГ у пацієнтів старшого віку.
2. При порівнянні пацієнтів за різними ознаками виявлено, що найбільш раннім та надійним маркером ураження нирок є протеїнурія. Частота АГ корелює зі ступенем нефропатії. Поява протеїнурії випереджає підвищення креатиніну у сироватці крові та зниження ШКФ.
3. У 5-річній перспективі появу протеїнурії можна очікувати у 25% пацієнтів із ССД, появу АГ — у 15%. Ризик розвитку нефропатії (АГ + протеїнурія) — 8%. Критичний термін появи симптомів ураження нирок — 3 роки.
Список використаної літератури
- Гусева Н.Г. (2002) Системная склеродермия: клиника, диагностика, лечение. Рос. журн. кож. и вен. болезней, 4: 5–15.
- Гусева Н.Г. (2007) Системная склеродермия: ранняя диагностика и прогноз. Науч.-практ. ревматол., 1: 39–45.
- Коваленко В.М., Корнацький В.М. (2014) Хвороби системи кровообігу як медико-соціальна і суспільно-політична проблема. Національний науковий центр «Інститут кардіології імені акад. М.Д. Стражеска», 262 с.
- Курята О.В., Лисунець Т.К., Шевцова А.І. та ін. (2006) Взаємозалежність між клінічним перебігом склеродермії та станом фібринонектину, ступенем його фрагментації. Укр. ревматол. журн., 4: 4–8.
- Наказ МОЗ України від 14.02.2002 р. № 54 (2002) Про затвердження класифікації захворювань органів системи кровообігу.
- Наказ МОЗ України від 02.12.2004 р. № 593 «Клінічний протокол надання медичної допомоги хворим із нефротичним синдромом» (2004) Про затвердження протоколів надання медичної допомоги за спеціальністю «Нефрологія».
- Наказ МОЗ України від 12.10.2006 р. № 676 «Клінічний протокол надання медичної допомоги хворим із системною склеродермією (ССД)» (2006) Про затвердження протоколів надання медичної допомоги за спеціальністю «Ревматологія».
- Реброва О.Ю. (2002) Статистический анализ медицинских данных. Применение пакета прикладных программ STATISTICA. МедиаСфера, Москва, 312 с.
- Abraham D.J., Krieg T., Distler J., Distler O. (2009) Overview of pathogenesis of systemic sclerosis. Rheumatology, 48: 3–7.
- Denton C.P., Lapadula G., Mouthon L., Müller-Ladner U. (2009) Renal complication and scleroderma renal crisis. Rheumatology, 48: 32–35.
- Haskova V., Haslik L., Riha F. et al. (1978) Evaluation of the level of circulating immune complexes by using polyethylenglycole. Immunitet farsch., 154(4): 134–144.
- Hunzelmann N., Genth E., Krieg T. et al. (2008) The registry of the German Network for Systemic Scleroderma: frequency of disease subsets and patterns of organ involvement. Rheumatology, 47: 1185–1192.
- Guillevin L., Bérezné A., Seror R. et al. (2012) Scleroderma renal crisis: a retrospective multicentre study on 91 patients and 427 controls. Rheumatology, 51: 460–467.
- LeRoy E.C., Medsger T.A.Jr. (2001) Criteria for the classification of early systemic sclerosis. Rheumatology, 28: 1573–1576.
- Levey A.S., Stevens L.A. (2009) A new equation to estimate glomerular filtration rate. Ann. Intern. Med., 150(9): 604–612.
- Mayes M.D. (2003) Scleroderma epidemiology. Rheum. Dis. Clin. North. Am., 29: 239–254.
- Shanmugamand V.K., Steen V.D. (2010) Renal manifestations in scleroderma: evidence for subclinical renal disease as a marker of vasculopathy. Intern. J. Rheumatol., Article ID 538589, 8 pages.
- Siva B., McDonald S.P., Hawley C.M. et al. (2011) End-stage kidney disease due to scleroderma—outcomes in 127 consecutive ANZDATA registry cases. Nephrol. Dial. Transplant., 28: 1–6.
- Silman A.J. (1991) Epidemiology of scleroderma. Ann. Rheum. Dis., 50: 846–853.
- Simeón-Aznar C.P., Fonollosa-Plá V., Tolosa-Vilella C. et al. (2012) Registry of the Spanish Network for Systemic Sclerosis: Clinical Pattern According to Cutaneous Subsets and Immunological Status. Semin. Arthritis Rheum., 41(6): 789–800.
- Solomon J.J., Olson A.L., Fischer A. et al. (2013) Scleroderma lung disease. Eur. Respir. Rev., 22(127): 6–19.
- Steen V.D., Costantino J.P., Shapiro A.P. et al. (1990) Outcome of renal crisis in systemic sclerosis: relation to availability of angiotensin-converting enzyme (ACE) inhibitors. Ann. Intern. Med., 113: 352–357.
- Steen V.D., Syzd A., Johnson J.P. et al. (2005) Kidney disease other than renal crisis in patients with diffuse scleroderma. J. Rheumatol., 32(4): 649–655.
- Varga J., Denton C.P., Wigley F.W. (2012) Scleroderma: from pathogenesis to comprehensive management. Springer, 687 р.
- Walker U.A., Tyndall A., Czirja´k L. et al. (2007) Clinical risk assessment of organ manifestations in systemic sclerosis: a report from the EULAR Scleroderma Trials And Research group database. Ann. Rheum. Dis., 66: 754–763.
РИСК РАЗВИТИЯ И ОСОБЕННОСТИ НЕФРОПАТИи У БОЛЬНЫХ СИСТЕМНОЙ СКЛЕРОДЕРМИей
Резюме. Исследовали риск развития и особенности течения нефропатии у больных системной склеродермией (ССД). В 5-летнем проспективном наблюдении участвовал 81 пациент с ССД. Участники находятся в региональном реестре, проходят регулярные обследования и получают медицинскую помощь в ревматологическом стационаре. Установлено, что у пациентов с диффузной ССД более выраженные фибротические изменения — пневмофиброз и уплотнения кожи, а у лиц с лимитированной ССД чаще определяли признаки сосудистой патологии — артериальной гипертензии (АГ). Наиболее ранним и надежным маркером поражения почек является протеинурия. Частота АГ коррелирует со степенью нефропатии.
системная склеродермия, артериальная гипертензия, протеинурия, нефропатия.
Адреса для листування:
Курята Олександр Вікторович
49044, Дніпропетровськ, вул. Дзержинського, 9
ДЗ «Дніпропетровська медична академія»
E-mail: gt1@dsma.dp.ua

Leave a comment