Клінічні особливості перебігу та оптимізація лікування остеоартрозу в поєднанні з абдомінальним ожирінням
Резюме. Проведено дослідження впливу абдомінального ожиріння (АОЖ) на перебіг остеоартрозу (ОА). Отримані результати підтверджують негативний вплив АОЖ на перебіг суглобового синдрому у хворих на ОА. При цьому у пацієнтів відзначають більш виражений больовий синдром, більш глибоке ураження суглобів, особливо нижніх кінцівок (100%), істотне збільшення кількості дефігурованих (припухлих) суглобів. Отримані результати можна пояснити не лише збільшенням навантаження на суглоби у зв’язку з надмірною масою тіла у пацієнтів, а й змінами на патогенетичному рівні перебігу ОА. За результатами анкетування встановлено, що АОЖ суттєво впливає на якість життя хворих на ОА. Причому у хворих на ОА погіршення відзначено за параметрами самообслуговування та біль/дискомфорт, а також за загальним індексом якості життя, а у пацієнтів із поєднаною патологією — за всіма показниками шкали EuroQol-5D, тобто більш суттєве наростання больового синдрому та погіршення якості життя. Вивчався вплив кверцетину та L-аргініну гідрохлориду на клініко-функціональний стан хворих на ОА у поєднанні з АОЖ. Отже, включення до традиційної протизапальної терапії кверцетину та L-аргініну гідрохлориду дозволяє покращити клініко-функціональний стан хворих на ОА у поєднанні з АОЖ та підвищити якість життя пацієнтів.
ВСТУП
Поширеність остеоартрозу (ОА), згідно з результатами спеціальних епідеміологічних досліджень, становить 643 випадки на 10 000 населення [3], а за даними статистичних звітів в Україні, — 220–240 на 10 000 людей (захворюваність — 49–52 на 10 000), причому ці показники щорічно зростають. Первинна інвалідність внаслідок ОА в Україні становить 0,8 на 10 000 населення [2]. Питання ранньої діагностики, профілактики і лікування цієї хвороби опорно-рухового апарату в нашій країні набувають особливої актуальності. У цьому зв’язку не можна не погодитися з Н. Вob та співавторами [9], що збільшення чисельності населення похилого віку призводить до підвищення поширеності ОА, що зумовлює серйозні медичні та соціально-економічні проблеми.
Патогенез ОА — складний і багатогранний. Проте сьогодні більшість експертів підтримують точку зору, що деградація суглобового хряща, перебудова субхондральної кістки і запалення є ключовими патогенетичними механізмами при ОА [7, 12]. Причому у конкретного хворого можуть переважати ті або інші патогенетичні фактори, що зумовлює особливості клінічних проявів захворювання (фенотип). Так, за наявності вираженого синовіту говорять про запальний фенотип ОА [9].
ОА зумовлений дією біологічних і механічних факторів, що дестабілізують нормальні відношення між процесами деградації та синтезу хондроцитів, позаклітинного матриксу суглобового хряща і субхондральної кістки [1]. Хрящова і кісткова тканини взаємозалежні, а тому зміни однієї з цих підсистем негайно відображаються на стані іншої. Механічне наднавантаження на суглоби спричиняє зниження резистентності хряща навіть до фізіологічного впливу, чому можуть сприяти інконгруєнтність артикулярних поверхонь унаслідок диспластичних змін.
Провідними патогенетичними факторами при ОА є дегенерація та деструкція суглобового хряща, що розвиваються внаслідок невідповідності між механічним навантаженням на суглобову поверхню хряща і його здатністю витримувати це навантаження [4]. З розпадом хряща фрагменти колагену і протеоглікани потрапляють у синовіальну рідину та ініціюють або підсилюють запальну реакцію у синовіальній тканині. Вони можуть також стимулювати вироблення запальних пептидів, індукувати аутоімунну відповідь організму і безпосередньо ушкоджувати хондроцити [10]. Запалення в суглобі асоціюється з рівнем цитокінів, які виявляють у синовіальній рідині хворих на ОА. Цитокіни, зокрема інтерлейкін-1β, стимулюють хондроцити, приводять до зростання синтезу метало- та серинових протеаз, гальмуючи синтез інгібіторів ензимів, і блокують синтез основних елементів матриксу — колагену та протеогліканів. У результаті відбувається підвищення активності протеаз, що в поєднанні з пригніченням синтезу хрящового матриксу веде до дегенерації хряща і прогресування ОА [11].
Згідно із сучасними даними [14], ожиріння — чинник ризику ОА і багатьох інших захворювань, пов’язаних із метаболічними порушеннями, а порушення функції та обмеження непрацездатності, що зазвичай супроводжують ОА, призводять до підвищення індексу маси тіла (ІМТ) та індукують розвиток кардіоваскулярних захворювань і діабету. Мета роботи — підвищити ефективність лікування хворих на ОА в поєднанні з абдомінальним ожирінням (АОЖ).
ОБ’ЄКТ І МЕТОДИ ДОСЛІДЖЕННЯ
У роботі наведено результати клінічного, лабораторно-інструментального обстеження та лікування 66 хворих на ОА у поєднанні з АОЖ, які перебували на стаціонарному лікуванні в ревматологічному відділенні Івано-Франківської обласної клінічної лікарні з 2011 по 2013 р. Діагностику ОА здійснювали згідно з наказом Міністерства охорони здоров’я (МОЗ) України від 12.10.2006 р. № 676 «Клінічний протокол надання медичної допомоги хворим із остеоартрозом». Наявність АОЖ у пацієнтів встановлювали на основі критеріїв, рекомендованих Міжнародною діабетичною федерацією (2005) [5]. Верифікацію діагнозу проводили на основі даних клінічних, лабораторних та інструментальних обстежень. Обстеження проводили тричі: при госпіталізації, на 10-й день лікування та після 30-го дня лікування.
Контрольну групу становили 20 осіб того ж віку, які в результаті проведення клінічних і додаткових досліджень були визнані практично здоровими, мали нормальні показники опорно-рухового апарату, ІМТ 19–24 кг/м, рівень ліпідів крові в межах норми. Середній вік у групі практично здорових осіб становив (49,92±1,96) року.
Також паралельно обстежено групу, до якої входили 15 пацієнтів з ОА без супутнього ожиріння. Середній вік у цій групі становив (48,79±1,94) року.
Клінічну характеристику проведено після ґрунтовного вивчення скарг, анамнезу хвороби і життя, даних об’єктивного обстеження, яке доповнювалось інструментальними методами аналізу функціонального стану опорно-рухового апарату і серцево-судинної системи, біохімічними і рентгенологічними дослідженнями.
Серед досліджуваних хворих на ОА з супутнім ожирінням переважали жінки — 47 (70,0%) особи, чоловіків було 19 (30,0%). Середній вік пацієнтів становив (59,18±1,26) року, тобто превалювали пацієнти працездатного віку, що підкреслює не лише медичне, але й соціальне значення проблеми діагностики й лікування ОА та ожиріння, середня тривалість захворювання становила — (9,82±0,62) року. Серед них: у 10 (15,15%) пацієнтів діагностовано І рентгенологічну стадію (Rtg-cтадію) ОА, у 26 (39,39%) — ІІ Rtg-стадію, 21 (31,82%) — ІІІ Rtg-стадію, а у 9 (13,64%) — ІV Rtg-стадію.
Середня маса тіла становила (99,31±1,46) кг, середній ІМТ становив (33,80±0,34) кг/м, середня окружність талії (ОТ) становила (104,65±0,64) см, середня окружність стегон (ОС) — (101,94±1,04) см, відношення ОТ/ОС у середньому становило (1,03±0,01).
Усі пацієнти з ОА, поєднаним з ожирінням, отримували базисну терапію (БТ), до якої входять нестероїдні протизапальні препарати (НПЗП), хондропротектори. У період лікування використовували раціональний режим та дієтичне харчування.
З метою вивчення ефективності запропонованих засобів пацієнтів розподілили на групи. У 1-й групі (n=17) — обстежувані отримували традиційну патогенетичну БТ, яка включала застосування одного із нижченаведених НПЗП — переважно селективні інгібітори циклооксигенази (ЦОГ)-2 (німесулід 200 мг у 2 прийоми, мелоксикам — 7,5–15 мг на 1 прийом, целекоксиб — 100 мг у 2 прийоми), неселективні інгібітори ЦОГ (диклофенак — 50 мг у 3 прийоми); хондропротектори — пероральний прийом хондроїтин сульфату 1000 мг/добу; фізіотерапевтичне лікування (лазеротерапія, магнітотерапія) протягом 1 міс. У 2-й групі пацієнтів (n=16) до БТ додано антиоксидантний препарат кверцетин у дозі 50 мг, розведений у 50 мл ізотонічного розчину, застосовували внутрішньовенно 1 раз на добу 5 днів, із переходом на пероральну його форму у дозі 40 мг 2 рази на добу до 1 міс. У 3-й групі (n=16) приймали БТ з додаванням амінокислоти L-аргініну гідрохлориду в дозі 100 мл 1 раз на добу 5 днів із переходом на пероральну його форму у вигляді сиропу по 5 мл 3 рази на добу протягом 1 міс. У 4-й групі (n=17) лікували препаратом БТ у комплексі з кверцетином та L-аргініну гідрохлоридом у вищезазначених дозах.
Контрольні обстеження проводилися до початку терапії, через 5 днів та через 1 міс після призначеного лікування. Критеріями ефективності терапії були самопочуття хворих, динаміка скарг та клінічної картини, рентгенологічні зміни, оцінка больового синдрому, показники якості життя, зміна показників ліпідного обміну, зміна показників цитокінового статусу та біомаркерів ОА.
Для клінічної оцінки функціонального стану опорно-рухового апарату нами використовувалися такі тести:
- оцінка кількості припухлих (дефігурованих) суглобів на підставі пальпації, а також характеру і вираженості больового синдрому в останніх, вираженого обмеження рухливості в них;
- вираженість болю оцінювали за 10-сантиметровою візуальною аналоговою шкалою (ВАШ). Цей тест відображав загальну вираженість суглобового болю за оцінкою хворого, де 0 означає відсутність болю, а 10 — максимальну інтенсивність болю. При цьому оцінювали окремо інтенсивність больового синдрому у спокої та у русі;
- індекс Lequesne включав оцінку болю у спокої та при ходьбі (5 запитань), максимально пройденої відстані (1 запитання) та повсякденної активності (4 запитання). Бальна оцінка кожного запитання підсумовувалася і становила рахунок тяжкості захворювання. Рахунок у межах 1–4 класифікувався як легкий ОА, 5–7 — помірний ОА, 8–10 — тяжкий ОА, 11–13 — дуже тяжкий ОА, >14 — вкрай тяжкий ОА [13];
- індекс WOMAC (Western Ontario and McMaster University) визначали за допомогою опитувальника для самостійної оцінки пацієнтом вираженості болю у спокої та при ходьбі (5 запитань), вираженості і тривалості скутості (2 запитання) і функціональної недостатності у повсякденній діяльності (17 запитань) [8].
Для визначення якості життя хворих на ОА використовували анкету EuroQol-5D, яка містить запитання щодо наявності труднощів під час ходьби, у самообслуговуванні, повсякденній діяльності, болю/дискомфорту, занепокоєння/депресії, ВАШ болю [3].
Отримані результати обробляли за допомогою програми «STAТISTICA 6.0» (StatSoftInc, США) та «Microsoft Excel» з обчисленням середньої величини М, середньоквадратичного відхилення, середньої помилки середньої величини m, значення вірогідності (p), коефіцієнта кореляції Спірмена (r). При нормальному розподілі використовуватиметься t-критерій Стьюдента і парний критерій Стьюдента.
РЕЗУЛЬТАТИ ДОСЛІДЖЕННЯ ТА ЇХ ОБГОВОРЕННЯ
При первинному обстеженні хворих на ОА і пацієнтів із поєднаною патологією з’ясувалося, що серед останніх суглобовий синдром був більш виражений, що підтверджують вірогідно вищі значення ВАШ, індексу Lequesne та WOMAC (табл. 1).
у поєднанні з АОЖ
| Показник | ОА | ОА + АОЖ |
|---|---|---|
| ВАШ, см | 2,63±0,38 | 5,21±1,15 |
| Індекс Lequesne, балів | 6,84±1,52 | 15,2±2,16 |
| Індекс WOMAC | 36,8±4,8 | 59,6±6,1 |
*р<0,05 між показниками у хворих на ОА та ОА + АОЖ.
У хворих із поєднаною патологією показник ВАШ був вищим у 2 рази порівняно із пацієнтами із ОА (р<0,05).
Індекс Lequesne залишається одним із найнадійніших для оцінки тяжкості ОА у хворих з ураженням великих суглобів. Цей показник у хворих на ОА в поєднанні з ожирінням перевищував у 2,2 раза відповідний показник у хворих на ОА (р<0,05), що свідчить про значний внесок приєднання АОЖ у посиленні проявів суглобового синдрому.
Індекс WOMAC дає можливість адекватно оцінити функціональний стан суглобів у хворих на ОА. Нами встановлено, що найвищий показник індексу WOMAC був у пацієнтів із поєднаною патологією, перевищуючи у 1,6 раза відповідно аналогічний показник у хворих на ОА (р<0,05).
Отримані клінічні результати підтверджено інструментальними методами обстеження. При рентгенологічному обстеженні у 8 (53,3%) пацієнтів лише із ОА діагностували І рентгенологічну стадію, у 5 (33,3%) — ІІ, у 2 (13,3%) — ІІІ стадію. Серед обстежених із ОА та АОЖ у 8 (11,7%) виявлено ОА І рентгенологічної стадії, у 29 (45,0%) — ІІ, у 23 (35,0%) — ІІІ та у 6 (8,3%) — ІV рентгенологічної стадії. Подібну динаміку виявлено при розподілі хворих залежно від клінічного варіанта ОА (рисунок).
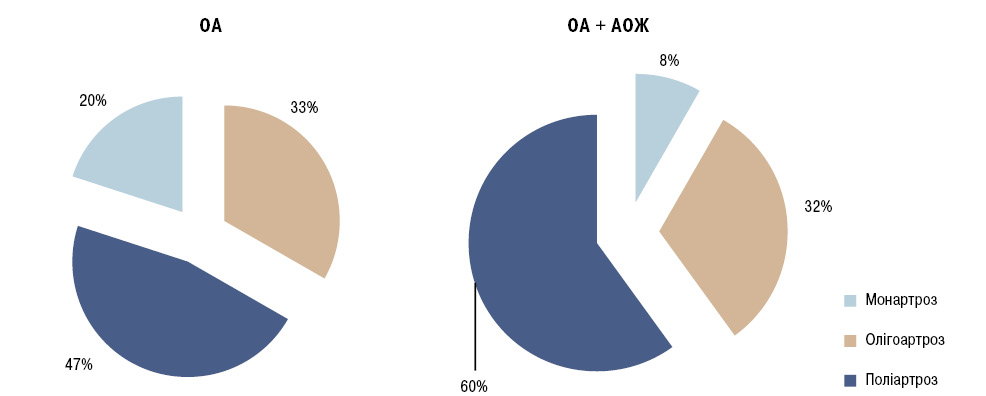
Так, моноостеоартроз виявлено у 5 (33,3%) хворих лише із ОА, олігоостеоартроз — у 7 (46,7%), поліостеоартроз — у 3 (20,0%) обстежених. Серед хворих на ОА та АОЖ виявлено найбільшу частку хворих на поліостеоартроз та олігоостеоартроз — 40 (60,0%) та 21 (31,7%) пацієнтів відповідно.
Рецидивний синовіт діагностовано у 3 (20,0%) пацієнтів із ОА та у 26 (43,3%) — із поєднаною патологією. Причому частота рецидивів прямо пропорційна тяжкості перебігу ОА і тривалості захворювання. Виявлено, що у осіб із ОА, асоційованим з ожирінням, частіше, ніж у хворих на ОА, уражені суглоби нижніх кінцівок (100 і 84,7% відповідно), особливо колінні суглоби (92,7 і 82,1% відповідно).
Дефігурованими виявлялися частіше суглоби нижніх кінцівок у всіх групах хворих, однак при аналізі цього показника серед пацієнтів з ознаками ожиріння частіше відзначали дефігуровані суглоби всіх локалізацій, особливо колінних суглобів (30 і 60,7% відповідно) і суглобів нижніх кінцівок (34,3 і 66,5% відповідно).
Отримані результати підтверджують негативний вплив АОЖ на перебіг суглобового синдрому у хворих на ОА. При цьому у пацієнтів відзначають більш виражений больовий синдром, більш глибоке ураження суглобів, особливо нижніх кінцівок (100%), істотно збільшується кількість дефігурованих (припухлих) суглобів. Отримані результати можна пояснити не лише збільшенням навантаження на суглоби, у зв’язку з надмірною масою тіла у пацієнтів, а й змінами на патогенетичному рівні перебігу ОА.
Оцінка якості життя в сучасній ревматології займає вагоме місце, що віддзеркалює, з одного боку, появу нових лікувальних технологій, які недостатньо впливають на тривалість життя хворих, але значно підвищують якість життя пацієнтів, а з іншого — підвищення активності хворого, його ролі у виборі методів діагностики та лікування.
За результатами анкетування встановлено, що АОЖ суттєво впливає на якість життя хворих на ОА. Відзначали негативну динаміку показників анкети якості життя пацієнтів (табл. 2). Так, у хворих на ОА у поєднанні з АОЖ встановлено, що показники фізичної активності (ходьба, самообслуговування, повсякденна активність) перевищували відповідні у пацієнтів на ОА у 1,4 та 1,7 раза відповідно (р<0,001), психологічного дискомфорту — у 1,5 раза (р<0,01) та загального індексу — у 1,8 раза (р<0,001) і, відповідно, зростання показників загального індексу EuroQol-5D у 1,5 раза (р<0,001) порівняно з відповідними показниками у хворих на ОА.
| Показник | ОА | ОА + АОЖ |
|---|---|---|
| Ходьба, балів | 1,08±0,05 | 1,57±0,07 |
| Самообслуговування, балів | 1,04±0,05 | 1,41±0,03 |
| Повсякденна активність, балів | 1,16±0,07 | 1,68±0,09 |
| Біль/дискомфорт, балів | 1,12±0,04 | 1,49±0,09 |
| Занепокоєння/депресія, балів | 0,98±0,06 | 1,49±0,05 |
| Індекс EuroQol-5D, балів | 5,38±0,12 | 8,04±0,17* |
*р<0,05 між показниками у хворих на ОА та ОА + АОЖ.
Причому, у хворих на ОА погіршення наявне за параметрами «самообслуговування» та «біль/дискомфорт», а також за загальним індексом якості життя, а у пацієнтів із поєднаною патологією — погіршення за всіма показниками шкали EuroQol-5D, тобто більш значне наростання больового синдрому та погіршення якості життя.
Таким чином, тяжкість клініко-функціонального стану хворих на ОА залежить від ступеня надмірної маси тіла.
Нами вивчався вплив кверцетину та L-аргініну гідрохлориду на клініко-функціональний стан хворих на ОА у поєднанні з АОЖ.
Пацієнти 1-ї групи отримували традиційну БТ, комплекс якої включав: НПЗП, хондропротектори, і симптоматичну терапію, рекомендовану наказом МОЗ України від 12.10.2006 р. № 676 «Про затвердження клінічних протоколів надання медичної допомоги хворим із остеоартрозом» [6]. Динаміку показників оцінювали на початку лікування, через 10 днів та через 1 міс після проведеної комплексної терапії (табл. 3).
| Показник | Група | ||||
|---|---|---|---|---|---|
| 1-ша | 2-га | 3-тя | 4-та | ||
| ВАШ, см | До лікування | 5,19±0,75 | 5,01±0,59 | 5,71±0,95 | 5,28±0,39 |
| 10-та доба | 4,30±0,55 | 3,93±0,57 | 3,97±0,45 | 3,51±0,86 | |
| 30-та доба | 4,01±0,19 | 3,11±0,67 | 3,59±0,53 | 2,71±0,59 | |
| Індекс Lequesne, балів | До лікування | 14,02±1,04 | 15,21±3,45 | 15,12±2,09 | 16,08±1,12 |
| 10-та доба | 11,92±3,04 | 11,02±2,11 | 11,09±1,90 | 10,82±1,02 | |
| 30-та доба | 10,52±1,22 | 9,25±2,02 | 9,31±1,20 | 8,42±1,81 | |
| Індекс WOMAC, балів | До лікування | 58,72±5,8 | 59,8±1,2 | 59,83±3,5 | 58,9±4,8 |
| 10-та доба | 50,2±5,8 | 48,14±1,5 | 48,22±6,1 | 45,09±1,8 | |
| 30-та доба | 45,7±2,8 | 41,78±3,6 | 41,87±4,02 | 38,7±3,7 | |
*р<0,05 між показниками до та після лікування.
На фоні отриманого лікування встановлено позитивну динаміку суглобового синдрому у досліджуваної групи хворих. При аналізі показників больового синдрому та функціонального стану хворих за анкетою WOMAC (біль у спокої та при навантаженні, утруднена рухливість, обмеження у щоденній діяльності) відзначено достовірне зниження всіх показників після курсу лікування від початку дослідження.
Так, на 10-ту добу спостереження у 1-й групі показники ВАШ були у 1,2 раза нижчими, індекс Lequesne — у 1,2 раза, WOMAC — у 1,2 раза порівняно з відповідними результатами обстеження до лікування (p<0,05). Подібну динаміку встановлено при обстеженні на 30-ту добу БТ. Показники ВАШ були нижчими у 1,3 раза, індекс Lequesne та WOMAC — у 1,3 та 1,3 раза відповідно, ніж до лікування (р<0,05).
У пацієнтів 2-ї та 3-ї групи також спостерігалася позитивна динаміка, а показники були схожі між собою. Так на 5-ту добу показники ВАШ були у 1,3 (2-га група) та 1,4 (3-тя група) рази нижчими, індекс Lequesne — у 1,4 раза у 2-й та 3-й групі, WOMAC — у 1,2 раза відповідно, порівняно з показниками до лікування (p<0,05). Позитивну динаміку встановлено і при обстеженні на 30-ту добу БТ в поєднанні з кверцетином, де спостерігали, що показники ВАШ у 1,6 раза, індекс Lequesne — у 1,7 раза, WOMAC — у 1,4 раза нижчі порівняно з відповідними результатами до лікування. Схожі результати спостерігалися у пацієнтів 3-ї групи, які на фоні БТ приймали L-аргініну гідрохлорид, показники ВАШ були у 1,6 раза, індекс Lequesne — у 1,6 раза та WOMAC — у 1,4 раза нижчі, ніж до лікування.
Найкращі результати спостерігались у пацієнтів 4-ї групи, що разом із БТ приймали кверцетин та L-аргініну гідрохлорид. Так, на 10-ту і 30-ту добу лікування показники ВАШ були у 1,5 та 1,9 раза нижчими, індекс Lequesne — у 1,5 та 1,9 раза, WOMAC — у 1,3 та 1,5 раза порівняно з відповідними результатами до лікування (p<0,05).
Тривалий больовий синдром, порушення функції суглобів та обмеження рухової активності, небажані побічні реакції на медикаментозну терапію, соціальні обмеження у хворих на ОА сприяють значному погіршенню якості життя. Тому одним із критеріїв ефективності запропонованих лікувальних комплексів було вивчення показників якості життя за анкетою EuroQol-5D.
Через 1 міс лікування 49 (76,7%) хворих 2; 3 та 4-ї групи відзначили покращення загального стану, рухової активності.
Так, у хворих, які отримували БТ, при обстеженні на 10-ту та 30-ту добу вірогідно зменшилися показники порушення ходьби у 1,1 та 1,2 раза (р<0,001), самообслуговування — у 1,1 та 1,2 раза (р<0,01), покращилася повсякденна активність у 1,1 та 1,3 раза (р<0,05) на фоні зниження індексу больового синдрому та дискомфорту в суглобах у 1,2 і 1,6 раза (р<0,01) та покращення показника психоемоційного стану у 1,1 та 1,3 раза (р<0,05). Відповідно до позитивної динаміки показників складових опитувальника EuroQol-5D встановлено зниження загального індексу у 1,2 та 1,7 раза (р<0,01). Після проведеної БТ, незважаючи на те, що клінічна ремісія досягнута у великої частини хворих, суб’єктивна оцінка загального самопочуття та якості життя виявилася невисокою.
Відзначено позитивні зрушення показників якості життя при обстеженні на 10-ту і 30-ту добу у хворих, які отримували кверцетин у складі комплексної терапії (2-га група) та L-аргінін гідрохлорид разом із БТ (3-тя група). Так, у пацієнтів 2-ї та 3-ї груп вірогідно знизився індекс EuroQol-5D у 1,5 та 2,1 раза (р<0,001) на фоні покращення показників ходьби у 1,1 та 1,4 раза (р<0,01), самообслуговування та рухової активності — у 1,1 та 1,5 раза (р<0,05), зменшення вираженості болю/дискомфорту — у 1,3 та 1,8 раза (р<0,01), покращення показника психоемоційного стану — у 1,2 та 1,6 раза (р<0,05). Додавання кверцетину та L-аргініну гідрохлориду позитивно вплинуло на такі показники, як симптоми ОА, обмеження фізичної діяльності та емоційна сфера.
Найкращу динаміку показників відзначали у пацієнтів 4-ї групи, які на фоні БТ приймали кверцетин і L-аргініну гідрохлорид. Так, на 10-ту і 30-ту добу терапії у хворих цієї групи вірогідно знизилися показники порушення ходьби у 1,2 та 1,7 раза (р<0,001), самообслуговування — у 1,2 та 1,5 раза (р<0,01), покращилася повсякденна активність у 1,2 та 1,9 раза (р<0,05) на фоні зниження індексу больового синдрому та дискомфорту в суглобах у 1,4 та 2,1 раза (р<0,01) та покращення показника психоемоційного стану у 1,3 та 1,7 раза (р<0,05). Відповідно до позитивної динаміки показників складових опитувальника EuroQol-5D встановлено зниження загального індексу у 1,6 та 2,6 раза (р<0,01).
Отже, включення до традиційної протизапальної терапії кверцетину та L-аргініну гідрохлориду дозволяє покращити клініко-функціональний стан хворих на ОА у поєднанні з ожирінням, а також покращити якість життя пацієнтів.
ВИСНОВКИ
1. Встановлено, що у хворих на ОА в асоціації з АОЖ порівняно з ізольованим перебігом ОА спостерігається зростання тяжкості та вираженості клінічних симптомів (зростання показників ВАШ у 2,0 раза, індексів Lequesne та WOMAC — у 2,7 та 1,7 раза відповідно), погіршується ефективність БТ та знижується якість життя пацієнтів (р<0,01).
2. БТ у хворих на ОА у поєднанні з АОЖ сприяє зменшенню вираженості больового синдрому, незначному зниженню маркерів ОА та покращенню якості життя.
3. Включення до комплексної терапії хворих на ОА в поєднанні з АОЖ кверцетину та L-аргініну гідрохлориду зумовлює потенціювання позитивних ефектів цих препаратів, сприяє більш вираженій динаміці клінічних, лабораторних та інструментальних показників, значному покращенню якості життя (на 85,55%; р<0,05), що обґрунтовує доцільність використання запропонованої схеми з метою підвищення ефективності лікування досліджуваних захворювань.
| Показник | Група | ||||
|---|---|---|---|---|---|
| 1-ша | 2-га | 3-тя | 4-та | ||
| Ходьба, балів | До лікування | 1,50±1,07 | 1,52±1,01 | 1,53±1,03 | 1,51±1,17 |
| 10-та доба | 1,40±0,55 | 1,33±0,57 | 1,30±0,45 | 1,21±0,86 | |
| 30-та доба | 1,21±0,19 | 1,11±0,67 | 1,05±0,53 | 0,91±0,59 | |
| Самообслуговування, балів | До лікування | 1,38±0,03 | 1,39±0,03 | 1,41±0,03 | 1,39±0,03 |
| 10-та доба | 1,29±0,52 | 1,23±1,39 | 1,25±1,01 | 1,18±1,33 | |
| 30-та доба | 1,14±0,05 | 1,01±1,03 | 1,04±1,50 | 0,92±0,16 | |
| Повсякденна активність, балів | До лікування | 1,60±0,11 | 1,58±1,22 | 1,56±0,04 | 1,58±1,03 |
| 10-та доба | 1,49±5,8 | 1,41±1,5 | 1,43±6,1 | 1,35±1,8 | |
| 30-та доба | 1,26±2,8 | 1,08±0,52 | 1,09±0,05 | 0,82±0,22 | |
| Біль/дискомфорт, балів | До лікування | 1,89±0,09 | 1,90±2,19 | 1,89±1,11 | 1,90±1,01 |
| 10-та доба | 1,61±0,27 | 1,52±1,50 | 1,54±0,09 | 1,40±0,41 | |
| 30-та доба | 1,19±0,22 | 1,04±1,16 | 1,05±1,55 | 0,91±0,17 | |
| Занепокоєння/депресія, балів | До лікування | 1,44±1,22 | 1,45±2,03 | 1,43±1,53 | 1,45±0,05 |
| 10-та доба | 1,34±1,02 | 1,26±0,22 | 1,27±0,73 | 1,16±1,22 | |
| 30-та доба | 1,12±0,05 | 0,92±1,15 | 0,94±0,95 | 0,86±0,17 | |
| Індекс EuroQol-5D, балів | До лікування | 10,08±0,07 | 11,21±0,27 | 10,58±1,17 | 11,19±0,12 |
| 10-та доба | 8,35±0,31 | 7,44±0,72 | 7,56±0,34 | 6,89±0,92 | |
| 30-та доба | 6,01±1,01 | 5,35±0,21 | 5,46±1,33 | 4,35±2,56 | |
*р<0,05 між показниками у хворих І, ІІ, ІІІ і IV групи обстежених до та після лікування;
СПИСОК ВИКОРИСТАНОЇ ЛІТЕРАТУРИ
- 1. Дроздов В.Н., Коломиец Е.В., Лазебник Л.Б. (2006) Сравнительная эффективность и безопасность применения кетопрофена, лорноксикама, нимесулида и целекоксиба у больных остеоартрозом. Русский медицинский журнал (РМЖ), 12(14): 844–848.
- 2. Коваленко В.Н., Борткевич О.П. (2005) Остеоартроз: Практ. руковод. Морион, Киев, 592с.
- 3. Ковалева О.Н., Беловол А.Н., Заика М.В (2005) Роль оксидативного стресса в кардиоваскулярной патологии. Журн. АМН України, 4: 660–670.
- 4. Королева С.В., Львов С.Е., Григорьев Э.В. и др. (2006) Медикаментозное лечение остеоартроза (обзор литературы). Травматол. ортопед. России, 3(41): 76–81.
- 5. Митченко Е.И. (2007) Метаболический синдром, сахарный диабет и сердечно-сосудистые заболевания. Укр. кардіол. журн., 5: 74–80.
- 6. Наказ МОЗ України від 12.10.2006 р. № 676 «Клінічний протокол надання медичної допомоги за спеціальністю «Ревматологія».
- 7. Beth Smith M.E., Nancy Lee J., Pharm D. et al. (2009) Drug class review HMG-CoA reductase inhibitors (statins) and fixed-dose combination products containing a statin final report update 5. Portland, Oregon, 128 p.
- 8. Blankenberg S., Yusuf S. (2006) The inflammatory hypothesis: any progress in risk stratification and therapeutic targets? Circulation, 114(15): 1557–1560.
- 9. Bob H., Sun M.D., Christopher W. еt al. (2007) New developments in osteoarthritis. Rheum. Dis. Clin. N. Am., 33: 135–148.
- 10. Brakenhielm E., Veitonmaki N., Cao R. et al. (2004) Adiponectin-induced antiangiogenesis and antitumor activity involve caspase-mediated endothelial cell apoptosis. Proc. Natl. Acad. Sci. USA, 01: 2476–2481.
- 11. Burrage P.S., Mix K.S., Brinckerhoff C.E. (2006) Matrix metalloproteinases: role in arthritis. Front. Biosci., 11: 529–543.
- 12. Calza S., Decarli A., Ferraroni M. (2008) Research article open access obesity and prevalence of chronic diseases in the 1999–2000 Italian National Health Survey. BMC Public Health, 14: 110–115.
- 13. Jordan K.M., Arden N.K., Doherty M. et al. (2005) EULAR evidence based recommendations for the management of hip osteoarthritis: report of a task force of the EULAR Standing Committee for International Clinical Studies Including Therapeutics (ESCISIT). Ann. Rheum. Dis., 64: 669–681.
- 14. Manek Nisha J., Hart D., Spector T.D. et al. (2003) The association of body mass index and osteoarthritis of the knee joint: an examination of genetic and environmental influences. Arthrit Rheum., 48: 1024–1029.
КЛИНИЧЕСКИЕ ОСОБЕННОСТИ ТЕЧЕНИЯ И ОПТИМИЗАЦИЯ ЛЕЧЕНИЯ ОСТЕОАРТРОЗА В сочетанИИ С АБДОМИНАЛЬНЫМ ОЖИРЕНИЕМ
Резюме. Проведено исследование влияния абдоминального ожирения (АОЖ) на течение остеоартроза (ОА). Полученные результаты подтверждают негативное влияние АОЖ на течение суставного синдрома у больных ОА. При этом у пациентов отмечают более выраженный болевой синдром, более глубокое поражение суставов, особенно нижних конечностей (100%), существенное увеличение числа дефигурированных (припухших) суставов. Полученные результаты можно объяснить не только увеличением нагрузки на суставы в связи с избыточной массой тела у пациентов, но и изменениями на патогенетическом уровне течения ОА. По результатам анкетирования установлено, что АОЖ существенно влияет на качество жизни больных ОА. Причем у больных ОА ухудшение отмечают по параметрам самообслуживание и боль/дискомфорт, а также по общему индексу качества жизни, а у пациентов с сочетанной патологией — ухудшение по всем показателям шкалы EuroQol-5D, то есть более значительное нарастание болевого синдрома и ухудшение качества жизни. Изучали влияние кверцетина и L-аргинина гидрохлорида на клинико-функциональное состояние больных ОА в сочетании с АОЖ. Итак, включение в традиционную противовоспалительную терапию кверцетина и L-аргинина гидрохлорида позволяет улучшить клинико-функциональное состояние больных ОА в сочетании с ожирением и повысить качество жизни пациентов.
остеоартроз, абдоминальное ожирение, ВАШ, WOMAC, Leqesne, кверцетин, L-аргинина гидрохлорид.
Адреса для листування:
Сухоребська Марія Ярославівна
76018, Івано-Франківськ, вул. Галицька, 2
ДВНЗ «Івано-Франківський національний медичний університет»,
кафедра внутрішньої медицини № 1,
клінічної імунології та алергології ім. Є.М. Нейка
E-mail: s_marya@mail.ru

Leave a comment