ОСНОВНІ ПРИНЦИПИ НОВИХ ДІАГНОСТИЧНИХ КРИТЕРІЇВ (2012) та РЕКОМЕНДАЦІЙ ACR/EULAR 2015 З МЕНЕДЖМЕНТУ І ЛІКУВАННя при РЕВМАТИЧНІй ПОЛІМІАЛГІЇ
Резюме. Ревматична поліміалгія — це запальне ревматичне захворювання, яке гостро розвивається і супроводжується вираженим симетричним болем у ділянці плечового й тазового пояса та шиї, обмеженням рухів, значним підвищенням гострофазових показників і анемією хронічного захворювання. Діагноз захворювання встановлюється клінічно, але потрібне проведення ретельної диференційної діагностики. У 2012 р. опубліковано класифікаційні критерії цього захворювання. У статті представлені основні положення нових клінічних рекомендацій 2015 р. щодо лікування ревматичної поліміалгії Американської колегії ревматологів та Європейської антиревматичної ліги (ACR/EULAR 2015). Представлено алгоритм ведення пацієнтів із ревматичною поліміалгією, обґрунтовано схеми застосування глюкокортикоїдів і графіки зниження дози. Рекомендації ACR/EULAR 2015 призначені, перш за все, для лікарів-клініцистів і прогнозується, що вони нададуть їм певну допомогу у веденні пацієнтів із ревматичною поліміалгією.
Ревматическая полимиалгия (РПМ)— (грец. Poly — много + Myalgia — мышечная боль) — воспалительное ревматическое заболевание, которое остро развивается и сопровождается выраженной симметричной болью в области плечевого, тазового пояса и шеи, ограничением движений, значительным повышением острофазовых показателей и анемией хронического заболевания [4]. РПМ является общим воспалительным ревматическим заболеванием людей пожилого возраста, и существует значительная неопределенность в ее диагностике. Дать короткое, но исчерпывающее определение этому заболеванию трудно, поскольку его уникальность, позволяющая отличить РПМ от других заболеваний, является исключительно клинической. Недаром авторы одной из последних обзорных статей R. Spiera и R. Westhovens, посвященных диагностике РПМ, сравнили это заболевание с порнографией. Они начинают свою статью этим ярким сравнением: «В 1964 г. судья Верховного суда США Поттер Стюарт, хорошо известный своими ораторскими способностями, когда пытался дать определение порнографии, сказал: «Я бы никогда не мог определить ее как следует, но я всегда узнаю ее, когда вижу». Ревматическая полимиалгия очень похожа на порнографию. Это синдром боли, воспаления, ограничения подвижности у людей старшего возраста, которому тяжело дать словесное определение, но с которым мы часто встречаемся в реальной клинической практике и который почти не пропускают опытные клиницисты». Статья данных ученых так и называется: «Ревматическая полимиалгия: выход за рамки клинической интуиции?» [15].
Первое описание пяти случаев РПМ было сделано шотландским врачом W. Bruce в 1888 г., он назвал эту болезнь «сенильной ревматической подагрой». Врач сообщил о 5 пациентах пожилого возраста, страдавших выраженной генерализованной миалгией, и указал, что клиническая картина в данных случаях отличалась от подагры, ревматизма и ревматоидного артрита, то есть от всех известных на то время заболеваний суставов [1]. Автором наиболее распространенного в настоящее время термина «ревматическая полимиалгия» является H. Barber, врач из Манчестера (1957). Несмотря на продолжающуюся критику данного термина, именно он прочно вошел в международный медицинский лексикон. Необходимо отметить, что во Франции более распространенным и употребляемым термином является «ризомелический псевдополиартрит», подчеркивающий поражение зон крупных суставов (плечевые и тазобедренные суставы) и отсутствие типичного артрита. Таким образом, с момента первого описания болезни прошло более 100 лет, однако до сих пор диагноз заболевания в основном устанавливают на основании яркой клинической картины.
Клиническая картина РПМ складывается из комбинации признаков поражения опорно-двигательного аппарата и изменений лабораторных показателей воспаления, которые наблюдаются у всех пациентов, а также общих (конституциональных) нарушений, возникающих часто, но не постоянно присутствующих [6]. Клинические особенности РПМ отображены в следующих положения:
- Начало заболевания — резкое, неожиданное, коварное; пик симптомов развивается достаточно быстро — через 2–3 нед.
- Основным клиническим симптомом выступает боль и скованность в плечевом и тазовом поясе, шее, что в большинстве случаев носит симметричный характер.
- Симптомы больше выражены утром.
- Характерен феномен геля — ощущение скованности после долгого периода отдыха или отсутствия активности.
- Общеконституционные симптомы — слабость, вялость, общее недомогание, депрессия, потеря массы тела, субфебрильная температура тела.
- Характерны артралгия и артрит суставов кистей, теносиновит кисти.
- Несмотря на наличие миалгии, нет мышечной слабости, боль не уменьшает также силу в конечностях, нет мышечной атрофии/гипотрофии.
- Определяется болезненность мышц при пальпации — от слабой до умеренной.
- Уменьшение диапазона движений в суставах, возможно, из-за боли.
- Могут присоединяться симптомы гигантоклеточного артериита. Единого мнения по вопросу взаимосвязи РПМ и болезни Хортона (гигантоклеточного артериита) нет. Она может быть начальным симптомом, возникать одновременно и появляться позже. Приблизительно у 15% пациентов с РПМ развивается гигантоклеточный артериит и 40–50% пациентов с гигантоклеточным артериитом имеют РПМ [3].
Лабораторные характеристики и особенности РПМ сгруппированы ниже:
- Существенное повышение скорости оседания эритроцитов (СОЭ) >50 мм/ч и С-реактивного белка (СРБ). СРБ при этом более чувствительный показатель, чем СОЭ.
- Анемия — нормохромная, нормоцитарная (анемия хронического заболевания).
- Миозитспецифические ферменты — креатининфосфокиназа, миоглобин, альдолаза — демонстрируют нормальные значения.
- Ревматоидный фактор негативный (следует помнить о возможности позитивного ревматоидного фактора у 5% лиц без признаков ревматического заболевания), антитела к циклическому цитруллированному пептиду (АЦЦП) — негативные.
- Антинуклеарные антитела — негативные.
- Отмечается значительное повышение уровня интерлейкин-6, что коррелирует с выраженностью воспаления.
- Возможно незначительное повышение печеночных тестов (аланинаминотрансфераза, аспартатаминотрансфераза, гамма-глутамилтранспептидаза).
Инструментальные методы исследования показали, что клиническая симптоматика РПМ обусловлена главным образом воспалительными изменениями суставов и околосуставных тканей. С помощью магнитно-резонансной томографии, ультразвукового исследования (УЗИ) и позитронной эмиссионной компьютерной томографии (ПЭТ-КТ) у больных РПМ выявляют признаки бурсита в области плечевых и тазобедренных суставов, а также шейного отдела позвоночника [7, 10]. Наиболее характерными являются поддельтовидный бурсит, теносиновит бицепса, трохантерный (вертлужный) бурсит, выпот в плечевом и/или тазобедренном суставах. Описан также синовит плечевых и тазобедренных суставов. При гистологическом исследовании синовиальной оболочки больных РПМ отмечают слабо выраженную воспалительную инфильтрацию с преобладанием макрофагов и CD4 Т-клеток [13].
На сегодняшний день не существует единственного клинического, лабораторного или инструментального признака, наличие которого позволяло бы подтвердить диагноз РПМ. Диагностику проводят по совокупности проявлений болезни. Наиболее типичные из них используют в качестве диагностических критериев, предложенных Европейской группой по изучению ревматической полимиалгии [10]. Они состоят из обязательных необходимых критериев, к которым относят возраст ≥50 лет, двустороннюю боль в плечах (появившуюся <12 нед назад), повышение СОЭ/CРБ. Критерии следует применять лишь в тех случаях, когда диагноз другого заболевания не представляется более обоснованным [4]. Для верификации диагноза и решения вопроса о назначении глюкокортикоидов (ГК) у таких пациентов могут быть использованы два набора критериев. При отсутствии данных УЗИ диагноз может быть подтвержден по 4 признакам: утренняя скованность >45 мин, боль или ограничение подвижности в тазобедренном суставе, отсутствие ревматоидного фактора и АЦЦП, отсутствие поражения других суставов. Максимально возможная сумма баллов по данным 4 критериям составляет 6. Для подтверждения диагноза РПМ достаточно набрать 4 балла.
Второй набор классификационных критериев используется при наличии результатов УЗИ и, помимо указанных основных четырех параметров, включает еще два дополнительных. Каждый дополнительный критерий представляет собой набор сонографических признаков. Первый из них предусматривает наличие как минимум поддельтовидного бурсита и/или теносиновита бицепса и/или синовита плечевого сустава (заднего или аксиллярного отдела), а также синовита тазобедренного сустава и/или трохантерного бурсита. Второй набор определяется как наличие двустороннего поддельтовидного бурсита, теносиновита бицепса или синовита плечевых суставов. Каждый из дополнительных критериев оценивается 1 баллом. Поэтому при использовании второго набора классификационных критериев максимально возможная сумма баллов составляет 8, и в этом случае для подтверждения диагноза РПМ необходимо набрать 5 баллов (таблица).
Обязательные критерии
|
||
| Критерий | Подсчет при отсутствии данных УЗИ (0–6 баллов) | Подсчет при наличии данных УЗИ (0–8 баллов) |
|---|---|---|
| Утренняя скованность >45 мин | 2 | 2 |
| Боль в области тазобедренных суставов или ограничение их подвижности | 1 | 1 |
| Отсутствие ревматоидного фактора и АЦЦП | 2 | 2 |
| Отсутствие поражений (боли) других суставов | 1 | 1 |
| Наличие как минимум одностороннего поддельтовидного бурсита и/или теносиновита бицепса, и/или синовита плечевого сустава (заднего или аксиллярного отдела) и как минимум — одностороннего синовита тазобедренного сустава, и/или трохантерного бурсита |
– | 1 |
| Наличие двустороннего поддельтовидного бурсита, теносиновита бицепса или синовита плечевых суставов | – | 1 |
Для подтверджения диагноза РПМ
|
||
На сегодняшний день существует множество расхождений в подходах к лечению пациентов с РПМ, которые включают вопросы дозирования ГК и целесообразности применения базисных болезнь-модифицирующих антиревматических препаратов (БМАРП) [5]. К сожалению, бо`льшая часть пациентов (29–45%) с РПМ не дают адекватного ответа на терапию ГК в течение первых 3–4 нед. При этом приблизительно у 50% больных отмечают разнообразные побочные эффекты на фоне лечения данной группой препаратов. Целью Американской коллегии ревматологов (ACR) и Европейской антиревматической лиги (EULAR) являлось обеспечение клиницистов кратким, четко изложенным современным руководством, которое поможет стандартизировать подходы к лечению и улучшить прогнозы для пациентов с данным заболеванием [11]. Как обычно, при создании подобных рекомендаций эксперты ACR и EULAR руководствовались доказательной методологией с использованием классов рекомендаций и уровней доказательности [2]. Алгоритм лечения пациентов с РПМ, основанный на рекомендациях (ACR/EULAR 2015), представлен на рисунке.
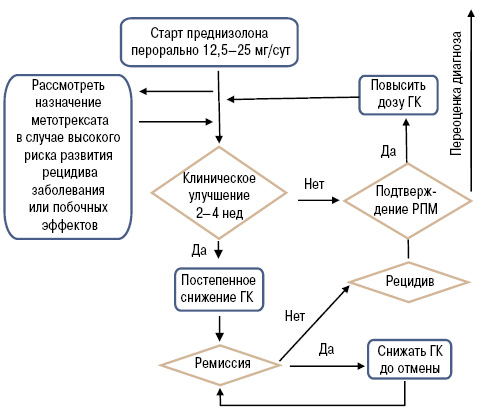
Экспертами тщательно проработана и обобщена вся база иcследований по РПМ и после детальной оценки и обсуждений изложена в окончательном варианте данных рекомендаций [11].
У всех пациентов, которые отвечают критериям РПМ, необходимо оценить коморбидность, применение других препаратов, а также факторы риска для возможных побочных эффектов в связи с планируемым длительным приемом ГК. Кроме этого, на старте назначения лечения необходимо оценить возможные факторы риска рецидива, что может обусловить большую длительность терапии ГК. Необходимо рассмотреть и оценить особые ситуации (опыт или риск побочных эффектов, рецидивы, атипичные проявления заболевания). Минимальный клинический и лабораторный набор данных должен быть документирован у каждого пациента перед назначением терапии.
Примерами сопутствующих заболеваний, связанных с повышенным риском развития ГК-ассоциированных побочных эффектов, являются артериальная гипертензия, сахарный диабет, нарушение толерантности к глюкозе, сердечно-сосудистые заболевания, дислипидемия, язвенная болезнь желудка, остеопороз (и, в частности, недавние переломы), наличие катаракты или глаукомы, наличие хронических или рецидивирующих инфекций, а также совместное назначение с нестероидными противовоспалительными препаратами (НПВП). Считается, что женский пол ассоциируется в большей степени с риском развития побочных эффектов, чем мужской [9]. Роль факторов риска в развитии рецидива/длительности терапии пока не ясна. Базовые факторы, которые были связаны с более высокой частотой рецидивов и / или длительной терапии в исследованиях, посвященных РПМ, были: женский пол [9], высокая СОЭ (более 40 мм/час) [8, 12], наличие периферического артрита [14].
Сами рекомендации состоят из 10 положений, представленных ниже [11]:
1. На старте терапии больным РПМ настоятельно рекомендуется использовать ГК вместо НПВП, за исключением возможного кратковременного применения НПВП и/или анальгетиков в случаях, когда болевой синдром ассоциирован с другой патологией (к примеру, сопутствующий остеоартрит).
2. Настоятельно рекомендуется использовать минимально эффективную индивидуальную длительность ГК-терапии у больных РПМ. Рекомендуется использовать график постепенного снижения дозы ГК (см. рекомендацию 4), что предполагает как минимум 12 мес лечения. Более конкретное утверждение не представляется возможным из-за отсутствия исследований по этой конкретной теме и из-за многочисленных подгрупп и факторов, которые необходимо учитывать при определении длительности терапии ГК.
3. Условно рекомендуется использовать минимально эффективную дозу ГК в диапазоне 12,5–25 мг преднизолона (или эквивалента) как стартового лечения при РПМ. Более высокая стартовая доза ГК в границах этого диапазона может рассматриваться у пациентов с высоким риском рецидива и низким риском побочных эффектов, в то же время, у пациентов с сопутствующими заболеваниями (например сахарный диабет, остеопороз, глаукома и др.) и другими факторами риска для ГК-ассоциированных побочных эффектов может быть лучшим назначение ГК в более низких дозах. Условно отрицается применение ГК в начальных дозах ≤7,5 мг/сут и настоятельно возражается против использования начальных доз >30 мг/сут.
4. Настоятельно рекомендуется индивидуализация графиков схождения с дозы ГК, основанных на регулярном мониторинге состояния пациента, активности заболевания, лабораторных маркеров и негативных событий. Предложены следующие принципы снижения доз:
А. Стартовое снижение: рекомендуется медленно снижать дозу ГК до 10 мг/сут в пересчете на преднизолон на протяжении 4–8 нед.
В. Терапия при рецидивах: рекомендуется повысить дозу перорального преднизолона до уровня, предшествовавшего рецидиву, и в последующем снижать ее постепенно (в течение 4–8 нед) до дозы, во время приема которой случился рецидив.
С. Снижение доз во время ремиссии: после достижения ремиссии необходимо снижать дозу преднизолона перорально на 1 мг каждые 4 нед (либо на 1,25 мг, используя, к примеру, схему 10/7,5 мг через день и т.д.) на протяжении того времени, пока сохраняется ремиссия.
5. Условно рекомендуется рассмотреть возможность внутримышечного введения метилпреднизолона как альтернативы пероральным ГК. Выбор между пероральным и внутримышечным введением остается на усмотрение врача. Рекомендации не могут четко указать фенотип пациента, который бы нуждался во внутримышечном введении ГК. Предложен следующий график схождения с дозы метилпреднизолона внутримышечно:
- Метилпреднизолон (депо-форма) внутримышечно 120 мг каждые 3 нед до 9-й недели.
- На 12-й неделе — 100 мг, с последующими 3-месячными интервалами.
- Далее дозу снижают на 20 мг каждые 12 нед до 48-й недели.
- После этого дозу снижают на 20 мг каждые 16 нед до полного прекращения.
В случае возникновения рецидива заболевания при схождении с дозы парентерального депо-метилпреднизолона рекомендуется переход на пероральный прием ГК с пересчетом дозы (повышение дозы до уровня ранее эффективной, то есть дорецидивной).
6. Условно рекомендуется использовать одноразовый, а не раздельный прием ежедневных доз ГК для лечения при РПМ. Разделять дозу препарата на несколько приемов следует в случае выраженного интенсивного болевого синдрома в ночное время суток.
7. Условно рекомендуется учесть возможность раннего применения метотрексата в дополнение к ГК, в частности у пациентов с высоким риском рецидива и/или при длительной терапии, а также в случаях имеющихся факторов риска, сопутствующих заболеваний и/или приема сопутствующих препаратов, когда высокая вероятность появления осложнений ГК-терапии или побочных эффектов ГК. В клинических испытаниях метотрексат применяли при пероральном применении в дозе 7,5–10 мг/нед.
8. Настоятельно рекомендуется не применять ингибиторы фактора некроза опухоли для лечения пациентов с РПМ. В настоящее время продолжается только одно рандомизированное клинических исследование с тоцилизумабом (clinicaltrials.gov NCT01396317), а также в другом исследовании сравнивается секукинумаб, канакинумаб и ГК (clinicaltrials.gov NCT01364389). К тому же, в случае назначения ингибиторов фактора некроза опухоли повышается риск негативного эффекта.
9. Условно рекомендуется рассмотреть создание индивидуальной программы упражнений для пациентов с РПМ, направленных на поддержание мышечной массы и функции, а также снижение риска падений.
10. Применение растительных препаратов в терапии РПМ не рекомендуется. Особенно категорически авторы документа выступают против использования китайских травяных препаратов Yanghe и капсул Biqi у пациентов с РПМ. Данное заявление связано, прежде всего, с тем, что вышеуказанные средства не одобрены Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) в США, а также Европейским агентством лекарственных средств (EMA).
Настоящие рекомендации [11] ACR/EULAR 2015 предназначены, прежде всего, для врачей-клиницистов и предполагается, что они окажут им определенную помощь в ведении пациентов с РПМ.
Список использованной литературы
- 1. Бунчук Н.В. (2010) Ревматические заболевания пожилых. МЕДпресс-информ, Москва, 272 с.
- 2. Ватутин Н.Т., Смирнова А.С., Тарадин Г.Г., Эль-Хатиб М.А. (2016) Обзор рекомендаций по лечению ревматической полимиалгии (EULAR/ACR 2015). Архивъ внутр. медицины, 1: 3–5.
- 3. Глазунов А.В., Жиляев Е.В., Толдиева Ф.А. (2006) Ревматическая полимиалгия и височный артериит. Клин. геронтология, 6: 34–46.
- 4. Олюнин Ю.А. (2013) Ревматическая полимиалгия. Consilium medicum, 15(9): 53–57.
- 5. Сатыбалдыев А.М. (2013) Лечение ревматической полимиалгии. Соврем. ревматол., 1: 66–72.
- 6. Щедрина И.С., Троицкая М.П., Овчаренко С.И. (2011) Ревматическая полимиалгия: сложности диагностики. Леч. врач, 4: 33–36.
- 7. Blockmans D., de Ceuninck L., Vanderschueren S. et al. (2007) Repetitive 18-fluorodeoxyglucose positron emission tomography in isolated polymyalgia rheumatica: a prospective study in 35 patients. Rheumatology (Oxford), 46(4): 672–677.
- 8. Cantini F., Salvarani C., Olivieri I. et al. (2000) Erythrocyte sedimentation rate and C-reactive protein in the evaluation of disease activity and severity in polymyalgia rheumatica: a prospective follow-up study. Semin Arthritis Rheum., 30: 17–24.
- 9. Cimmino M.A., Parodi M., Caporali R., Montecucco C. (2006) Is the course of steroid-treated polymyalgia rheumatica more severe in women? Ann. NY Acad. Sci., 1069: 315–321.
- 10. Dasgupta B., Cimmino M., Maradit-Kremers H. et al. (2012) 2012 provisional classification criteria for polymyalgia rheumatica: a European League Against Rheumatism/American College of Rheumatology collaborative initiative. Ann. Rheum. Dis., 71(4): 484–492.
- 11. Dejaco C., Singh Y., Perel P. et al. (2015) 2015 Recommendations for the management of polymyalgia rheumatica: a European League Against Rheumatism. American College of Rheumatology collaborative initiative Ann. Rheum. Dis., 74: 1799–1807.
- 12. Lee J.H., Choi S.T., Kim J.S. et al. (2013) Clinical characteristics and prognostic factors for relapse in patients with polymyalgia rheumatica (PMR). Rheumatol. Int., 33: 1475–1480.
- 13. Meliconi R., Pulsatelli L., Uguccioni M. et al. (1996) Leukocyte infiltration in synovial tissue from the shoulder of patients with polymyalgia rheumatica. Quantitative analysis and influence of corticosteroid treatment. Arthritis Rheum., 39(7): 1199–1207.
- 14. Salvarani C., Cantini F., Macchioni P. et al. (1998) Distal musculoskeletal manifestations in polymyalgia rheumatica: a prospective followup study. Arthritis Rheum. 41:1221–1226.
- 15. Spiera R., Westhovens R. (2012) Provisional diagnostic criteria for polymyalgia rheumatica: moving beyond clinical intuition? Ann. Rheum. Dis., 71(4): 475–476.
Адрес для переписки:
Головач Ирина Юрьевна
03680, Киев, ул. Академика Заболотного, 21
Клиническая больница «Феофания» ГУД
E-mail: goloachirina@yandex

Leave a comment