Вивчення ефективності селективних нестероїдних протизапальних препаратів у хворих на остеоартроз
Шуба Н.М.1, Воронков Л.Г. 2, Воронова Т.Д.1, Пилипенко А.В.1, Гуленко О.І.1, Литвиненко С.В.1
- 1Національна медична академія післядипломної освіти ім. П.Л. Шупика, Київ
- 2ГУ «ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины», Киев
Резюме. У статті представлена порівняльна характеристика найпоширеніших лікарських засобів групи селективних нестероїдних протизапальних препаратів, зокрема німесуліду та мелоксикаму. Результати дослідження продемонстрували переваги німесуліду, які проявились у швидкому клінічному, протизапальному ефекті, і на відміну від мелоксикаму, у зниженні рівня оксиду азоту, що може свідчити про зменшення запального процесу та деградації хрящової тканини, а також про сприятливий профіль безпеки протягом 2 тиж, що дозволяє рекомендувати його як препарат вибору в купіруванні больового синдрому при остеоартрозі.
Остеоартроз (ОА) — хроническое прогрессирующее заболевание суставов с поражением прежде всего гиалинового хряща и субхондральной кости в результате сложного комплекса биомеханических, биохимических и/или генетических факторов. ОА вовлекает в орбиту патологического процесса прежде всего нагрузочные (коленные и тазобедренные) суставы и этим значительно ухудшает качество жизни больных, приводя к инвалидизации (Bruyere O. et al., 2014).
В настоящее время предложено большое количество международных и национальных рекомендаций по лечению пациентов с ОА. Наибольший интерес представляют рекомендации Европейского общества по клиническим и экономическим аспектам остеопороза и остеоартроза (Тhe European Society for Clinical and Economic Aspects of Osteoporosis and Osteoarthritis — ESCEO), предложенные в 2014 г. В каждом конкретном клиническом случае выбор рациональной терапии при ОА определяется различными показателями, в частности эффективностью и безопасностью лекарственных препаратов, коморбидным фоном пациента, предикторами ответа на проводимую терапию, темпами рентгенологического прогрессирования, параметрами, влияющими на основные патогенетические аспекты заболевания.
Нестероидные противовоспалительные препараты (НПВП) относятся к числу наиболее назначаемых и важных «симптоматических» лекарственных средств. Это определяется оригинальным сочетанием противовоспалительных, анальгезивных, жаропонижающих свойств, перекрывающих почти весь спектр основных симптомов, наиболее характерных для воспалительных заболеваний (Martiel-Pelletier J. et al., 2003). В последних рекомендациях Международного общества по изучению ОА (The Osteoarthritis Research Society International — OARSI) 2016 г. применение селективных НПВП при ОА более эффективно в сравнении с неселективными НПВП.
Нимесулид является препаратом с мультифакторным механизмом действия, которое не ограничивается только ингибирующим влиянием на синтез циклооксигеназы (ЦОГ)-2. ЦОГ-независимые эффекты нимесулида прежде всего заключаются в ингибировании активности NO-синтазы и, соответственно, образовании оксида азота (NO) и пероксинитрита (ОNOO), которые являются ключевыми медиаторами в процессе разрушения клеток организма и элементами воспалительного ответа. По последним данным установлено, что нимесулид угнетает in vivo высвобождение фактор некроза опухоли (TNF) и продукцию активного кислорода — два эффекта, которые вносят существенный вклад в противовоспалительное и анальгезивное действие препарата (Bennet A., Villa G., 2000). Поскольку ОА возникает у лиц с сопутствующей кардиоваскулярной патологией, и такие особенности нимесулида, как активация синтеза ингибитора тканевого активатора плазминогена, блокирование синтеза тромбоцитактивирующего фактора, являются чрезвычайно важными в предупреждении тромбоэмболических осложнений (Lane N.E. et al., 2011). Нимесулид подавляет активность 5-липоксигеназы, таким образом снижая риск возникновения воспаления, язвообразования в желудочно-кишечном тракте, препятствует бронхоконстрикции, что делает данный препарат более безопасным в отношении гастроинтестинальных осложнений и препаратом выбора у пациентов с бронхообструктивным синдромом (Laporte J.R. et al., 2004).
Мелоксикам характеризуется противовоспалительным, обезболивающим и жаропонижающим действием, которое связано с селективным ингибированием изофермента ЦОГ-2. При этом он структурно отличается от других ЦОГ-2-ингибиторов, вследствие чего связывается с верхней частью канала ЦОГ-2, а не с боковой частью этого фермента (Чичасова Н.В., 2011). Мелоксикам легко проникает в синовиальную жидкость, где его концентрация составляет 45–57% концентрации в плазме крови, обладает выгодными фармакокинетическими свойствами. Длительный период полувыведения (Т½=20 ч) позволяет назначать препарат 1 раз в сутки, что делает его удобным в применении и способствует строгому соблюдению пациентами режима лечения (Warksman J.C., 2007).
В настоящее время остается актуальным вопрос о дифференцированном подходе в купировании болевого синдрома у больных ОА с учетом как клинической эффективности препарата, так и его безопасности и переносимости.
Цель исследования — изучение эффективности и безопасности применения нимесулида и мелоксикама у больных ОА.
Объект и методы исследования
Ранее на базе терапевтического отделения Центральной городской клинической больницы (ЦГКБ) № 7 проведено исследование по изучению эффективности и безопасности нимесулида у больных ОА. При анализе данных, в частности показателей воспалительного процесса, получены интересные результаты в отношении уровня NO с 5,33±0,72 до 3,19±0,34 через 2 нед применения нимесулида, TNF-α с начального уровня до лечения 45,6±14,08 до 16,26±1,6 через 14 дней применения препарата (р<0,05) (Шуба Н.М. и соавт., 2016). Это стало основанием для проведения сравнительного анализа клинической эффективности, безопасности и переносимости таких препаратов, как нимесулид и мелоксикам, одних из наиболее назначаемых и применяемых лекарственных препаратов у больных ОА.
На базе терапевтического отделения ЦГКБ № 7 обследовано 40 больных с подтвержденным ОА клинически (критерии Американского колледжа ревматологов (ACR), 1990) и рентгенологически (I–III рентгенологическая стадия по Kellgren — Lawrence).
Пациентов распределили на две группы. В 1-й группе (n=20) пациентам назначен гранулированный нимесулид в саше по 100 мг 2 раза в сутки в течение 2 нед. Во 2-й группе (n=20) пациенты принимали мелоксикам в таблетках в дозе 15 мг 1 раз в сутки в течение 2 нед.
Для оценки выраженности болевого синдрома использовали визуальную аналоговую шкалу (ВАШ), оценивали альгофункциональный индекс Lequesne, индекс WOMAC (Western Ontario and McMaster Universities osteoarthritis index). Лабораторное обследование 1-й и 2-й группы пациентов включало: общеклинический анализ крови и мочи, из биохимических показателей выполнены: глюкоза крови, билирубин, трансаминазы (аланинаминотрансфераза (АлАТ), аспартатаминотрансфераза (АсАТ)), креатинин, С-реактивный белок (CRP); иммунологические методы исследования крови включали: исследование уровня NO, интерлейкина (IL)-1B, инсулиноподобного фактора роста (IGF)-1. Рентгенографию коленных суставов проводили по стандартной методике в переднезадней и боковой проекциях. Рентгенологическую стадию устанавливали согласно классификации Kellgren — Lawrence.
При анализе применяли методы описательной статистики (вычисляли такие показатели: среднее арифметическое значение (M), ошибка среднего (m), стандартное отклонение (SD), минимум, максимум), определяли достоверность различий по t-критерию Стьюдента.
Для статистической обработки данных использовали программно-математический комплекс «Microsoft Exel» и компьютерные программы для статистического анализа «Биостатистика», «SPSS Statistics», в частности непараметрический тест: критерий знаковых рангов — критерий Уилкоксона.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
На фоне проводимой терапии отмечено достоверное уменьшение выраженности болевого синдрома по ВАШ в обеих группах, в 1-й группе — на 35,6%, во 2-й группе — на 13,34%. При оценке альгофункционального индекса Lequesne выявлено статистически достоверное уменьшение выраженности боли в 1-й группе на 30,3% через 2 нед приема нимесулида, а во 2-й группе, принимавшей мелоксикам, — на 25,7% через 2 нед лечения (табл. 1).
в результате лечения нимесулидом и мелоксикамом
| Показатель | Нимесулид | Мелоксикам | ||||||
|---|---|---|---|---|---|---|---|---|
| До лечения | Через 2 нед | До лечения | Через 2 нед | |||||
| Me | IQR | Me | IQR | Me | IQR | Me | IQR | |
| ВАШ, мм | 57,5 | 53,5–65,5 | 35* | 31,25–42,25 | 60,00 | 57,00–67,00 | 55,00* | 45,00–60,00 |
| WOMAC, мм: | ||||||||
| Боль | 193,00 | 117,5–340,25 | 91,00* | 48,75–160,75 | 342,50 | 51,75–434,75 | 197,00* | 26,25–261,50 |
| Скованность | 100,00 | 76,75–111,00 | 68,5* | 48,00–88,00 | 93,00 | 14,00–107,50 | 64,00* | 11,25–87,75 |
| Функциональная недостаточность | 725,00 | 332,25–1167,75 | 414,00* | 166,25–734,00 | 646,00 | 64,00 | 436,50* | 44,25–577,00 |
| Индекс Lequesne, баллов | 9,5 | 8,00–12,75 | 6,5* | 5,25–9,00 | 11,00 | 8,00–14,00 | 8,00* | 6,00–11,00 |
| Показатели воспалительного процесса: | ||||||||
| NO, мкмоль/л | 4,81 | 3,19–7,27 | 3,05* | 2,5–4,68 | 3,10 | 0,43–6,97 | 2,98 | 0,40–6,60 |
| CRP, мг/л | 5,59 | 2,7–14,03 | 2,66* | 1,04–7,55 | 7,81 | 4,49–17,36 | 3,80* | 1,86–11,36 |
| IL-1B, пг/мл | 22,63 | 12,75–34,15 | 17,06* | 11,08–29,84 | 23,95 | 17,43–32,43 | 23,54 | 17,32–32,58 |
| IGF-1, нг/мл | 9,4 | 2,71–47,01 | 9,6 | 2,85–50,25 | 18,77 | 1,69–85,69 | 21,00 | 2,07–91,00 |
*р<0,001 при использовании критерия Уилкоксона.
| Показатель | Нимесулид | Мелоксикам | ||
|---|---|---|---|---|
| До лечения | Через 2 нед | До лечения | Через 2 нед | |
| Динамика болевого синдрома по ВАШ, мм | 57,1±3,16 | 36,8±1,56* –35,6% |
62,2±2,39 | 53,9±2,44* –13,4% |
| WOMAC, мм: | ||||
| Боль | 222,15±26,65 | 102,35±14,07* –53,9% |
278,4±40,6 | 174,55±27,19* –37,3% |
| Скованность | 100,5±7,92 | 70,7±7,68* –29,7% |
74,5±11,05 | 59,65±9,43* –20% |
| Функциональная недостаточность | 732±104,5 | 427,8±65,3* –1,6% |
515±79,0 | 377,9±62,3* –26,6% |
| Индекс Lequesne, баллов | 10,55±0,75 | 7,35±0,59* –30,3% |
11,67±1,1 | 8,67±0,86* –25,7% |
| Показатели воспалительного процесса: | ||||
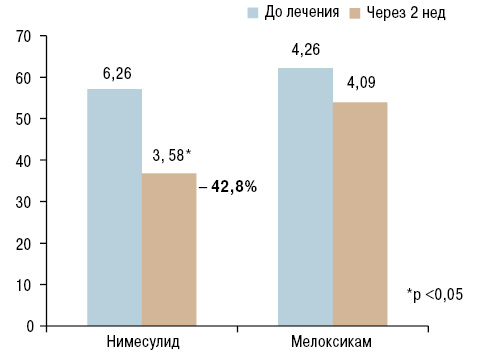
| NO, мкмоль/л | 6,26±0,98 | 3,58±0,44* –42,8% |
4,26±0,94 | 4,09±0,91 |
| CRP, мг/л | 12,99±4,12 | 4,75±1,2* –63,4% |
12,72±2,94 | 6,3±1,28* –50,48% |
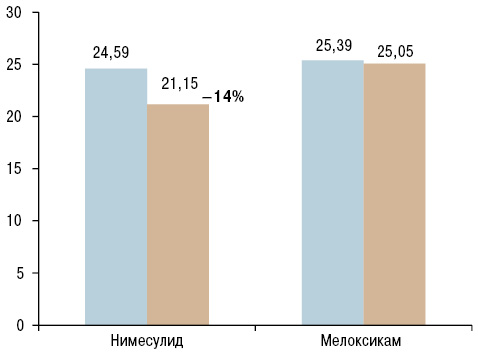
| IL-1B, пг/мл | 24,59±2,88 | 21,15+2,78* –14% |
25,39±2,9 | 25,05±2,86 |
| IGF-1, нг/мл | 23,53±6,36 | 25,6±6,42 | 44,65±11,47 | 46,26±11,73 |
*р<0,05 при использовании t-критерия Стьюдента.
Боль, скованность, функциональные нарушения оценены также с помощью анкеты WOMAC (см. табл. 1). На фоне лечения пациенты 1-й группы отметили повышение физической активности и значительное улучшение двигательного режима, что находит отражение в достоверном уменьшении выраженности боли на 53,9%, скованности — на 29,7% и функциональных нарушений — на 41,6%. У пациентов 2-й группы интенсивность уменьшения выраженности боли, скованности и функциональных нарушений была менее выраженной: боль — на 37,3%, скованность — на 20%, функциональные нарушения — на 26,6% через 2 нед лечения.
Учитывая весомый вклад в развитие воспалительного процесса при ОА таких мощных индукторов воспаления, как IL-1B и NO, представлялось важным провести сравнительную характеристику данных показателей в обеих группах. Получены следующие результаты: в 1-й группе статистически достоверное снижение уровня IL-1B на 14% (рис. 1), а также NO — с 6,26±0,98 до 3,58±0,44 (42,8%) (рис. 2) через 14 дней приема нимесулида, в то время как во 2-й группе, принимавшей мелоксикам, не выявлено статистически достоверного снижения уровня NO и IL-1B, что может указывать на ингибирующее влияние нимесулида на NO, IL-1B и более выраженную противовоспалительную активность в сравнении со 2-й группой, где уровень данных показателей практически не изменялся на фоне лечения мелоксикамом, но в то же время и не повышалась их концентрация в крови.
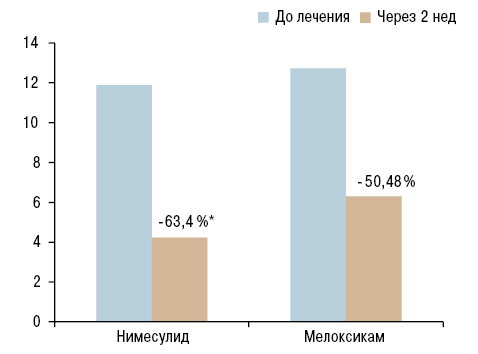
С учетом существенного влияния CRP на течение ОА, одного из основных показателей тяжести воспалительного процесса, нами отмечено статистически достоверное снижение уровней CRP в плазме крови в обеих группах (в 1-й группе на 64,4%, во 2-й группе — на 50,48%) что может указывать на снижение воспалительного ответа в обеих группах.
При анализе результатов в обеих группах не выявлено статистически достоверного повышения уровней IGF-1, обладающего анаболическим действием, что диктует необходимость как на фоне применения нимесулида, так и мелоксикама добавлять к лечению структурно-модифицирующие препараты для достижения стойкой клинической ремиссии, а также замедления дальнейшего прогрессирования деструкции хрящевой ткани.
Результаты анализа данных биохимических показателей крови (билирубин, АлАТ, АсАТ, глюкоза, креатинин) свидетельствуют о том, что ни в 1-й, ни во 2-й группе статистически достоверного изменения данных не выявлено (табл. 3).
| Показатель | 1-я группа | 2-я группа | ||
|---|---|---|---|---|
| До лечения | Через 2 нед | До лечения | Через 2 нед | |
| Билирубин, мкмоль/л | 17,59±0,55 | 17,59±0,55 | 17,01±0,9 | 16,81±0,89 |
| АлАТ, мккат/л | 0,12±0,007 | 0,13±0,009 | 0,19±0,02 | 0,19±0,02 |
| АсАТ, мккат/л | 0,17±0,05 | 0,17±0,05 | 0,18±0,022 | 0,21±0,026 |
| Глюкоза, ммоль/л | 5,1±0,16 | 5,05±0,12 | 5,03±0,22 | 5,14±0,23 |
| Креатинин, мкмоль/л | 92,6±3,24 | 92,2±2,74 | 90,9±1,94 | 91,1±2,13 |
Необходимо отметить, что в 1-й группе на фоне применения нимесулида в течение 14 дней побочных явлений не выявлено, в то время как во 2-й группе в начале терапии мелоксикамом (от 3 до 5 дней) у 5 пациентов отмечены такие побочные реакции, как постоянная тошнота, однократная рвота, болевой синдром и ощущение дискомфорта в животе, в связи с чем они прекратили свое участие в данном исследовании и, соответственно, были из него исключены.
ВЫВОДЫ
Результаты анализа применения селективных НПВП свидетельствуют о достоверном клиническом эффекте в обеих группах, однако нимесулид, в отличие от мелоксикама, оказывает более выраженный клинический эффект, а именно: уменьшение выраженности болевого синдрома, скованности и функциональных нарушений, что, возможно, связано с его коротким механизмом действия (Т½ — 3,2–6 ч), в то время как мелоксикам обладает более пролонгированным механизмом действия (Т½ — 15–20 ч).
Нимесулид и мелоксикам показали выраженный противовоспалительный эффект по данным CRP, одного из основных показателей тяжести течения воспалительного процесса.
В группе нимесулида и мелоксикама отмечена тенденция к повышению уровня IGF-1, обладающего анаболическим эффектом, что может указывать на возможный хондропротекторный эффект данных препаратов.
Изучение эффективности нимесулида и его влияния на отдельные медиаторы воспаления, а именно достоверное снижение уровня TNF, NO, IL-1B, и биохимические данные, свидетельствуют о его высокой эффективности и безопасности.
При применении нимесулида, в отличие от применения мелоксикама, выявлено снижение NO, основного индуктора воспаления и деградации хрящевой ткани при ОА.
Нимесулид показал достаточный профиль безопасности и переносимости по сравнению с мелоксикамом, при применении которого выявлены гастроинтестинальные побочные эффекты у 5 пациентов.
Учитывая вышеизложенное, при выборе селективного НПВП для быстрого купирования болевого синдрома у пациентов с ОА предпочтение можно отдавать нимесулиду.
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
- Чичасова Н.В. (2011) Мелоксикам в лечении хронических заболеваний опорно-двигательного аппарата. Ревматология, 4: 11.
- Шуба Н.М., Воронова Т.Д., Пилипенко А.В., Литвиненко С.В. (2016) Эффективность нимесулида и его влияние на отдельные катаболические и анаболические факторы у больных остеоартрозом. Укр. ревматол. журн., 1(63): 57–60.
- Bennet A., Villa G. (2000) Nimesulid: an NSAID that preferentially inhibits COX-2, and has various unique pharmacological activities. Exp. Opin. Pharmacother., 1: 277–286.
- Bruyere O., Cooper C., Pelletier J.P. et al. (2014) An algorithm recommendation for the management of knee osteoarthritis in Europe and internationally: A report from a task force of the European Society for Clinical and Economic Aspects of Osteoporosis and Osteoarthritis (ESCEO). Semin. Arthritis Rheum., 44(3): 253–263.
- Lane N.E., Brandt K., Hawker G. et al. (2011) OARSI-FDA initiative: defining the disease state of Osteoarthritis. Osteoarth. Cartil., 19(5): 478–482.
- Laporte J.R., Ibanez L., Vidal X., Vendrell L., Leone R. (2004) Upper Gastrointestinal Bleedings, Associated with the Use of NSAIDs, Drug Safety, 27(6): 411–420.
- Martiel-Pelletier J., Zajeunesse D. et al. (2003) Therapeutic role of dual inhibitors of 5-Zox & Cox, selective and non-selective non-steroidal anti-inflammatory drugs. Ann. Rheum. Dis., 62: 501–509.
- Warksman J.C. (2007) Nonselective nonsteroidal anti-inflammatory drugs and cardiovascular risk: are they safe? Ann. Rharmacother., 41: 1163–1173.
Адрес для переписки:
Шуба Неонила Михайловна
04112, Киев, ул. Дорогожицкая, 9
Национальная медицинская академия
последипломного образования им. П.Л. Шупика

Leave a comment